
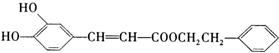 )是一种天然抗癌药物,在一定条件下能发生如下转化:
)是一种天然抗癌药物,在一定条件下能发生如下转化: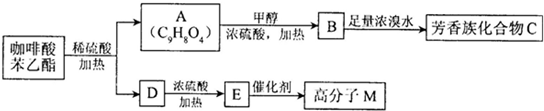
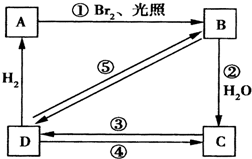
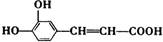 ,A→B发生酯化反应,则B为
,A→B发生酯化反应,则B为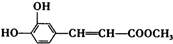 ,B中含C=C和酚-OH,B→C发生加成反应和取代反应;D为
,B中含C=C和酚-OH,B→C发生加成反应和取代反应;D为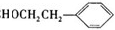 ,D→E发生消去反应,E为苯乙烯,E→M发生加聚反应,则M为
,D→E发生消去反应,E为苯乙烯,E→M发生加聚反应,则M为 ,据此答题;
,据此答题; ,A→B发生酯化反应,则B为
,A→B发生酯化反应,则B为 ,B中含C=C和酚-OH,B→C发生加成反应和取代反应;D为
,B中含C=C和酚-OH,B→C发生加成反应和取代反应;D为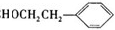 ,D→E发生消去反应,E为苯乙烯,E→M发生加聚反应,则M为
,D→E发生消去反应,E为苯乙烯,E→M发生加聚反应,则M为 ,
,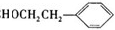 ,则官能团为羟基,
,则官能团为羟基, ,
, ;
; ,
, ;
; ,A的同分异构体中同时符合①苯环上只有两个取代基;②能发生银镜反应,说明有-CHO基团;③能与碳酸氢钠溶液反应,说明有-COOH基团;④能与氯化铁溶液发生显色反应,说明含酚羟基,符合这样的结构有
,A的同分异构体中同时符合①苯环上只有两个取代基;②能发生银镜反应,说明有-CHO基团;③能与碳酸氢钠溶液反应,说明有-COOH基团;④能与氯化铁溶液发生显色反应,说明含酚羟基,符合这样的结构有 、
、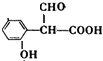 、
、 ,共3种,
,共3种, 或
或 或
或 ;
;


科目:高中化学 来源: 题型:
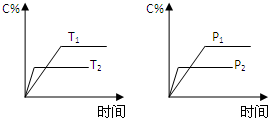 可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图下列叙述正确的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图下列叙述正确的是( )| A、达平衡后,若升温,平衡左移 |
| B、达平衡后,加入催化剂则C%增大 |
| C、化学方程式中a+b>c+d |
| D、达平衡后,减少A的量有利于平衡向右移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35.5g超氧化钾(KO2)所含的阴离子中电子数为8NA |
| B、标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA |
| C、常温常压下,92g NO2和N2O4混合气体中含有的原子数为6NA |
| D、工业上铜的电解精炼时电解池中每转移1mol电子时阳极上溶解的铜原子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com