
分析 (1)存在的分子有H2O、H2A,则H2A为弱酸;
(2)等体积混合生成Na2A,水解显碱性,离子水解以第一步为主;由反应式Ba2++A2-=BaA↓可得:沉淀后A2-过量0.01mol,溶液中c(A2-)=$\frac{0.01mol}{30×1{0}^{-3}L}$=$\frac{1}{3}$mol•L-1,根据BaA的Ksp可得c(Ba2+);
(3)①弱酸电离,②中水解生成分子,③中等体积混合为等量的NaCl、NaHA、H2A,浓度均为0.01mol/L,抑制弱酸的电离;
(4)混合溶液c(H+)/c(OH-)=104,c(H+)=10-5mol/L,显酸性,则酸过量,以此分析.
解答 解:(1)存在的分子有H2O、H2A,则H2A为弱酸,电离方程式为H2A?H++HA-、HA-?H++A2-,故答案为:H2A?H++HA-、HA-?H++A2-;
(2)等体积混合生成Na2A,水解显碱性,pH>7,离子水解以第一步为主,则离子浓度关系为c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+),由反应式Ba2++A2-=BaA↓可得:沉淀后A2-过量0.01mol,溶液中c(A2-)=$\frac{0.01mol}{30×1{0}^{-3}L}$=$\frac{1}{3}$mol•L-1,根据BaA的Ksp=c(Ba2+)•c(A2-)可得c(Ba2+)=$\frac{Ksp}{c({A}^{2-})}$=$\frac{1.8×1{0}^{-10}}{\frac{1}{3}}$=5.4×10-10 mol•L-1;
故答案为:>;c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);5.4×10-10;
(3)①弱酸电离,②中水解生成分子,③中等体积混合为等量的NaCl、NaHA、H2A,浓度均为0.01mol/L,抑制弱酸的电离,则三种情况的溶液中H2A分子浓度最大的为③,最小的为②,②溶液pH大于③,①③相比①的酸性强,则pH最小,所以②>③>①,故答案为:③;②>③>①;
(4)混合溶液c(H+)/c(OH-)=104,c(H+)=10-5mol/L,显酸性,则酸过量,H2A为弱酸,pH=3的H2A溶液与pH=11的NaOH溶液混合时酸的浓度大于碱的浓度,则二者体积关系不确定,大于、小于或等于都可能酸过量,故答案为:均有可能.
点评 本题考查较综合,涉及酸碱混合的定性分析、pH、电离与水解、电离方程式等,把握溶液中的溶质及电离与水解的趋势、相互影响即可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,18 g H2O含有的原子数为NA | |
| B. | 1.8 g的NH4+离子中含有的电子数为0.1 NA | |
| C. | 常温常压下,11.2 L氧气所含的原子数为NA | |
| D. | 2.4 g金属镁变为镁离子时失去的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
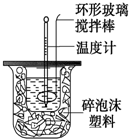 测定中和反应反应热的实验装置如图所示,实验结果产生偏差的原因不可能是( )
测定中和反应反应热的实验装置如图所示,实验结果产生偏差的原因不可能是( )| A. | 实验中使用的搅拌棒材料为铁 | |
| B. | 读取温度计读数时,读取的是混合溶液的最高温度 | |
| C. | 分多次把NaOH溶液倒入盛有硫酸的小烧杯中 | |
| D. | 用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合物 | B. | 氧化物 | C. | 醋酸盐 | D. | 钠盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com