
| A£® | v£ØA2£©=1.5 mol/£ØL•s£© | B£® | v£ØB2£©=2.4 mol/£ØL•s£© | C£® | v£ØC£©=1.6 mol/£ØL•s£© | D£® | v£ØA2£©=6 mol/£ØL•min£© |
·ÖĪö ÓÉÓŚ²»Ķ¬ĪļÖŹ±ķŹ¾µÄĖŁĀŹÖ®±ČµČÓŚ»Æѧ¼ĘĮæŹżÖ®±Č£¬¹Ź²»Ķ¬ĪļÖŹÖŹ±ķŹ¾µÄ·“Ó¦ĖŁĀŹÓėĘä»Æѧ¼ĘĮæŹżµÄ±ČÖµŌ½“ó£¬Ōņ±ķŹ¾µÄ·“Ó¦ĖŁĀŹŌ½æģ£®
½ā“š ½ā£ŗA.$\frac{v£Ø{A}_{2}£©}{1}$=1.5 mol/£ØL•s£©£»
B.$\frac{v£Ø{B}_{2}£©}{3}$=0.8 mol/£ØL•s£©£»
C.$\frac{v£ØC£©}{2}$=0.8mol/£ØL•s£©£»
D.$\frac{v£Ø{A}_{2}£©}{1}$=6mol/£ØL•min£©=0.1mol/£ØL•s£©£¬
¹Ź·“Ó¦ĖŁĀŹv£ØA2£©£¾v£ØC£©=v£ØB2£©£¾v£ØD£©£¬
¹ŹŃ”A£®
µćĘĄ ±¾Ģā漲鷓ӦĖŁĀŹæģĀż±Č½Ļ£¬ÄŃ¶Č²»“ó£¬æÉŅŌ×Ŗ»ÆĪŖĶ¬Ņ»ĪļÖŹ±ķŹ¾µÄĖŁĀŹ½ųŠŠ±Č½Ļ£¬×¢Ņāµ„Ī»ŅŖĶ³Ņ»£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C3H6ŗĶC3H8 | B£® | C4H6ŗĶC3H8 | C£® | C5H12ŗĶC6H6 | D£® | C3H6ŗĶC3H8O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ū¢Ü¢Ż | B£® | ¢Ü¢Ż¢ß | C£® | ¢Ü¢Ż | D£® | ¢Ū¢Ü¢Ż¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

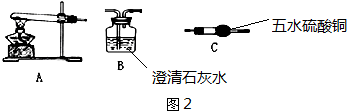

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻĖĪ¬ĖŲ”¢ÕįĢĒ”¢ĘĻĢŃĢĒŗĶÖ¬·¾ŌŚŅ»¶ØĢõ¼žĻĀ¶¼æÉ·¢ÉśĖ®½ā·“Ó¦ | |
| B£® | ·Ö×ÓŹ½ŹĒC3H8OµÄĖłÓŠĶ¬·ÖŅģ¹¹Ģå¹²3ÖÖ | |
| C£® | ÓĆŅŅ“¼ŗĶÅØH2SO4ÖʱøŅŅĻ©Ź±£¬²»æÉÓĆĖ®Ō”¼ÓČČæŲÖĘ·“Ó¦µÄĪĀ¶Č | |
| D£® | ĆŌµüĻćĖį½į¹¹ČēĶ¼£ŗ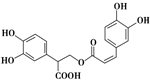 1 mol ĆŌµüĻćĖį×ī¶ąÄÜŗĶŗ¬6 mol NaOHµÄĖ®ČÜŅŗĶźČ«·“Ó¦ 1 mol ĆŌµüĻćĖį×ī¶ąÄÜŗĶŗ¬6 mol NaOHµÄĖ®ČÜŅŗĶźČ«·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
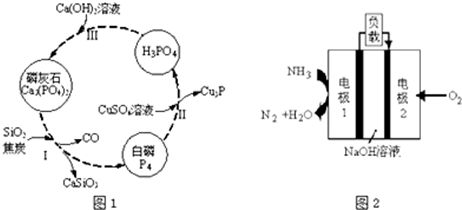
| A£® | Cu2SŹĒ»¹Ō²śĪļ£¬·“Ó¦ÖŠ1 mol CuSO4Ź§1 molµē×Ó | |
| B£® | 5 mol FeS2·¢Éś·“Ó¦£¬ÓŠ10 molµē×Ó×ŖŅĘ | |
| C£® | ²śĪļÖŠµÄSO42-Ąė×ÓÓŠŅ»²æ·ÖŹĒŃõ»Æ²śĪļ | |
| D£® | FeS2Ö»×÷»¹Ō¼Į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓŠ»śĪļ²»ÄÜĶعżČĖ¹¤µÄ·½·ØŗĻ³É | |
| B£® | ĢžŹĒÖøČ¼ÉÕŗóֻɜ³ÉCO2ŗĶH2OµÄÓŠ»śĪļ | |
| C£® | ÓŠ»śĪļÖ»ŗ¬ÓŠĢ¼”¢ĒāĮ½ÖÖŌŖĖŲ | |
| D£® | ŗ¬Ģ¼ŌŖĖŲµÄ»ÆŗĻĪļ²»Ņ»¶Ø¶¼ŹōÓŚÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
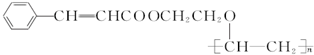 £®°“ČēĶ¼ĖłŹ¾¹ŲĻµæÉŅŌŗĻ³É¼×£¬ĘäÖŠŹŌ¼ĮIæÉÓÉŅŅ“¼ÓėŃõĘųŌŚ“߻ƼĮ¼ÓČČĢõ¼žĻĀ·“Ó¦µĆµ½£®
£®°“ČēĶ¼ĖłŹ¾¹ŲĻµæÉŅŌŗĻ³É¼×£¬ĘäÖŠŹŌ¼ĮIæÉÓÉŅŅ“¼ÓėŃõĘųŌŚ“߻ƼĮ¼ÓČČĢõ¼žĻĀ·“Ó¦µĆµ½£®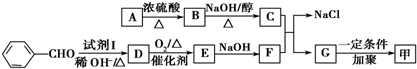
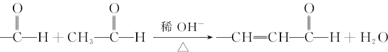
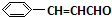 +O2$”ś_{”÷}^{“߻ƼĮ}$2
+O2$”ś_{”÷}^{“߻ƼĮ}$2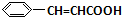 +H2O£»
+H2O£»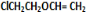 +
+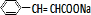 $\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$
$\stackrel{Ņ»¶ØĢõ¼ž}{”ś}$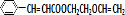 +NaCl£®
+NaCl£®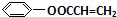 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com