
| A、胶体粒子直径在1nm-100nm之间 |
| B、胶体可发生丁达尔效应 |
| C、胶体粒子不能透过半透膜 |
| D、胶体粒子能够发生布朗运动 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、同温同压下,相同体积的物质,其物质的量一定相等 |
| B、不同的外界条件下,等物质的量的甲烷和一氧化碳所含的分子数不一定相等 |
| C、14g一氧化碳气体一定比20 g氧气的体积小 |
| D、相同条件下的一氧化碳气体和氮气,若体积相等,则分子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.7 g羟基所含电子的数目为NA |
| B、0.1 mol丙烯醛中含有双键的数目为O.1NA |
| C、室温时,pH=13的1.0 L Ba(OH)2溶液中含有OH-的数目为0.2NA |
| D、标准状况下,7.8 g苯中含氢原子的数目为O.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡溶液和稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| B、浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2↑ |
| C、SO2通入溴水中:SO2+Br2+2H2O=SO42-+2Br-+4H+ |
| D、钠放于水中:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、晶体硅、石墨都属于单质 |
| B、Na2O、Al2O3均为碱性氧化物 |
| C、醋酸、纯碱都属于强电解质 |
| D、水晶、水玻璃都属于盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
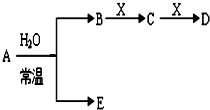 已知如图是常见元素形成的单质或化合物A、B、C、D、E、X转化关系(部分生成物和反应条件略去)
已知如图是常见元素形成的单质或化合物A、B、C、D、E、X转化关系(部分生成物和反应条件略去)查看答案和解析>>
科目:高中化学 来源: 题型:
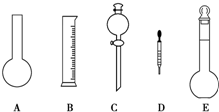 碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:
碳酸钙可以降低胃酸的浓度而被用作胃药的抗酸剂.某中学研究性学习小组为测定一胃药中碳酸钙的含量,设计了如下的实验操作:查看答案和解析>>
科目:高中化学 来源: 题型:
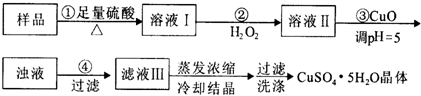
| A、利用CuCO3替代CuO也可调节溶液的pH,不影响实验结果 |
| B、步骤②中发生的主要反应为:H2O2+2Fe2++2H+=2Fe3++2H2O |
| C、洗涤:向装晶体的漏斗中加水至浸没晶体,待自然流下后重复2~3次 |
| D、某实验需要240 mL1mol/L的CuSO4溶液,则配制时需称量CuSO4?5H2O 60g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com