
| A. | 水、二氧化硫和干冰都属氧化物 | B. | H2SO4、HNO3和H2CO3都属于酸 | ||
| C. | KNO3、CuSO4和NH4Cl都属于盐 | D. | 烧碱、纯碱、熟石灰都属于碱 |
分析 A.氧化物是由两种元素组成,其中一种是氧元素的化合物;
B.电离出的阳离子全部是氢离子的化合物属于酸;
C.金属阳离子(或铵根离子)与酸根离子形成的化合物属于盐;
D.电离出的阴离子全部是氢氧根离子的化合物属于碱.
解答 解:A.水、二氧化硫和干冰都是由两种元素组成,其中一种是氧元素的化合物属氧化物,故A正确;
B.H2SO4、HNO3和H2CO3电离出的阳离子全部是氢离子,都属于酸,故B正确;
C.KNO3、CuSO4和NH4Cl是由金属阳离子(或铵根离子)与酸根离子形成的化合物都属于盐,故C正确;
D.纯碱即碳酸钠,是由金属阳离子与酸根离子形成的化合物属于盐,不是碱,故D错误.
故选D.
点评 本题考查物质的分类,了解常见物质的组成、物质的名称、分类,抓住各概念的特征进行分析判断是解答此类题的关键,属基础知识考查题,难度不大.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:填空题
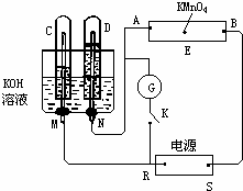
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向能使PH试纸显深蓝色的溶液中通入少量二氧化碳:OH-+CO2═HCO3- | |
| B. | 向NaClO溶液中加入浓氢溴酸:ClO-+2H++2 Br-═Cl-+Br2+H2O | |
| C. | 向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O═2HClO+CO32- | |
| D. | 向FeBr2溶液中滴加少量HClO溶液:2Fe2++HClO═2Fe3++Cl-+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
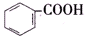 >H2CO3>
>H2CO3>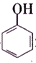 >HCO${\;}_{3}^{-}$,现将
>HCO${\;}_{3}^{-}$,现将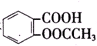 转变为
转变为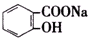 ,可行的方法是( )
,可行的方法是( )| A. | 向该溶液中加入足量的稀硫酸,加热 | |
| B. | 将该物质与稀硫酸共热后,再加入足量的NaOH溶液 | |
| C. | 将该物质与稀硫酸共热后,再加入足量的Na2CO3溶液 | |
| D. | 将该物质与足量的NaOH溶液共热,再通入足量CO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在一定条件下,使煤和氢气作用,可以得到液体燃料,也可以获得洁净的燃料油 | |
| B. | (CH3)2CHCH(CH3)2的系统命名为:2,3-二甲基丁烷 | |
| C. | 硬脂酸甘油酯可以在稀硫酸中水解,也可以在NaOH溶液中发生皂化反应彻底水解 | |
| D. | 氨基酸分子中均含有氨基和羧基,加入浓的硫酸钠溶液可从溶液中析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲型H1N1流感病毒是一种油脂 | |
| B. | 我们所吃的豆腐中主要含有蛋白质 | |
| C. | 棉花和蚕丝的主要成分都是纤维素 | |
| D. | 糯米中的淀粉一经发生水解反应就酿造成酒 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Y、z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:
Y、z为同周期金属元素,Y、Z的最高价氧化物对应水化物可以反应生成盐和水.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②④ | C. | ②⑤ | D. | ①⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com