
| A. | 14C可用于文物的年代鉴定,14C与13C互为同素异形体 | |
| B. | 最外层电子数为2的元素一定是金属元素 | |
| C. | 过渡元素一定是金属元素 | |
| D. | 同一周期中的第ⅡA族和第ⅢA族元素的原子序数差一定为1或11 |
分析 A、质子数相同中子数不同的原子互称同位素;
B、氦最外层是2个电子;
C、过渡元素含副族和第ⅤⅢ族元素;
D、根据元素所在周期表中的位置判断.
解答 解:A、13C和14C质子数相同中子数不同,互为同位素,故A错误;
B、氦最外层是2个电子,但为非金属元素,故B错误;
C、过渡元素含副族和第ⅤⅢ族元素,则一定为金属元素,故C正确;
D、第二、三周期的第ⅡA族和第ⅢA族元素的原子序数相差1,第四、五周期的第ⅡA族和第ⅢA族元素的原子序数相差11,第六、七周期的第ⅡA族和第ⅢA族元素的原子序数相差25,故D错误;
故选C.
点评 本题考查较为综合,侧重于元素周期表与周期律的考查,涉及同位素、周期表与周期律的关系及利用,题目难度中等,易错点为D,注意把握元素周期表的结构特点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 易溶于水的电解质一定是强电解质,难溶于水的电解质一定是弱电解质 | |
| B. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| C. | NaCl溶液在电流的作用下电离成钠离子和氯离子 | |
| D. | 氯化钠晶体不导电是由于氯化钠晶体中不存在自由移动的离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
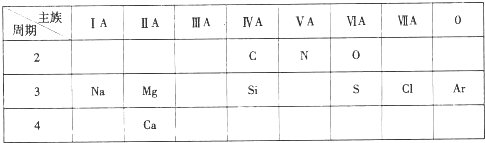
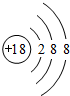 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2分子中所有原子最外层均达到8电子稳定结构 | |
| B. | NH4Cl、MgCl2均为离子化合物,均含有离子键和共价键 | |
| C. | 同周期第ⅠA族元素和第ⅦA族元素之间只能形成离子化合物 | |
| D. | NH4Cl仅由非金属元素组成,所以它是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羰基硫分子为非极性分子 | |
| B. | 羰基硫的结构式为:O=C=S | |
| C. | 羰基硫沸点比CO2高 | |
| D. | 羰基硫分子中三个原子处于同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内质子数为19 | B. | 原子核外电子数为19 | ||
| C. | 质量数为40 | D. | 中子数为40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16g | B. | 32g | C. | 126g | D. | 142g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com