
| ||
| ||
| ||
| 2.24L |
| 22.4L/mol |
| 1 |
| 2 |


 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����FeCl3��Һ�м���NaOH��Һ������ֺ��ɫ���� |
| B��������ˮ |
| C����ijЩ��̬�����������ɢ�ڲ������Ƴ���ɫ���� |
| D���峿�����Ǿ������������ï�ܵ���ľ֦Ҷ�������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D |
| ����ˮ�����Ȼ�̼�Ļ���� | ̽��̼���ƺ�̼�����Ƶ����ȶ��� | ��ȡ������������ | ��ȡ���ռ����� |
 |  |  |  |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��8.7g����������50mL 8mol?L-1Ũ����������ȡ���� |
| B��19.2gͭ��100mL 12mol?L-1�����ᷴӦ |
| C�������£���5.4g��ƬͶ��20mL 18mol?L-1�������� |
| D����������Cu����50mL 18mol?L-1 H2SO4��Һ�м��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ˮ����ͨ�����ȵ����ۣ����۱��ɫ |
| B����Fe��OH��3�����еμ�ϡH2SO4���ȳ��ֳ�����������ܽ� |
| C��������ʳ������ˮ���μӵ�����Һ������ɫ��˵�����Ǽӵ��� |
| D��Cu�Ľ��������Ա�Fe������ˮ����բ���Ͻ�װͭ��ɼ�������ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
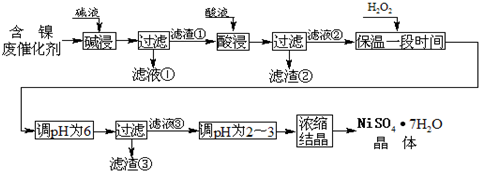
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com