
NaF、NaI、MgO均为离子化合物,现有下列数据,试判断三种化合物的熔点、沸点高低的顺序是
物质 | ①NaF | ②NaI | ③MgO |
离子电荷数 | 1 | 1 | 2 |
离子的核间距 | 23.1nm | 31.8nm | 21.0nm |
A.①>②>③ B.③>②>① C.③>①>② D.②>①>③
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源:2014-2015四川省资阳市高一上学期学期期末化学试卷(解析版) 题型:实验题
(6分)某待测液中可能含有Ba2+、Fe3+、K+、Fe2+、CO32-、Cl-等离子,进行如下实验:
①取适量待测液于试管中,加入稀H2SO4,有白色沉淀生成;
②过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;
③在步骤②中的溶液中,继续滴加氯水,溶液立即变红。
根据实验现象回答:
(1)待测液中一定含有的离子是 ,一定不含有的离子是 ;
(2)还有一种离子不能确定是否存在,要确认这种离子的实验方法和现象是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省资阳市高二上学期学期期末化学试卷(解析版) 题型:选择题
关于晶体的下列说法中正确的是
A.溶质从溶液中析出是得到晶体的三条途径之一
B.区别晶体和非晶体最好的方法是观察是否有规则的几何外形
C.水晶在不同方向上的硬度、导热性、导电性相同
D.只有无色透明的固体才是晶体
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:填空题
用单线桥表示下列反应中原子间得失电子情况:5KI+KIO3+3H2SO4→3K2SO4+3I2+3H2O
对上述反应,__________发生了氧化反应,________元素被还原了,若有415g KI发生反应,则被还原的碘元素为________g,转移的电子数为__________mol。
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
用下列实验装置和方法进行相应实验,能达到实验目的的是
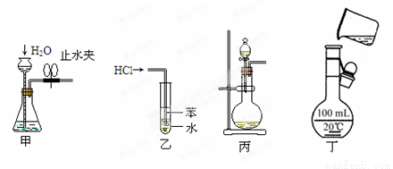
A.用图甲所示方法检查装置的气密性
B.乙图装置可用于吸收HCl气体,并防止倒吸
C.大理石和稀硫酸反应制CO2时选用丙图装置
D.用丁图所示装置将溶液定容到100mL
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列变化过程中,原物质分子内共价键被破坏,同时有离子键形成的是
A.盐酸和氢氧化钠反应 B.氯化氢溶于水
C.溴化氢和氨反应 D.锌和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市高一上学期期末考试化学试卷(解析版) 题型:选择题
金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关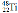 和
和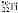 的说法中正确的是
的说法中正确的是
A.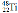 和
和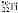 原子中均含有22个中子
原子中均含有22个中子
B.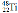 和
和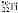 质子数相同
质子数相同
C.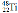 和
和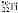 质量数不同,不能互称同位素
质量数不同,不能互称同位素
D.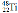 和
和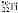 化学性质不同
化学性质不同
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市丰台区高三一模理综化学试卷(解析版) 题型:选择题
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
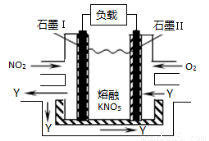
A.O2在石墨Ⅱ附近发生氧化反应
B.该电池放电时NO3-向石墨Ⅱ电极迁移
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3-
NO+ 2NO3-
D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广西玉林市博白县高三下学期返校调研考试化学试卷(解析版) 题型:填空题
(14分)“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K= 。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值_______(填具体值或取值范围)。
③实验4,若900 ℃时,在此容器中加入CO、H2O、CO2 、H2均为1 mol,则此时V正 V逆(填“<”,“>”,“=”)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g) = H2O(l) ΔH=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________
(3)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。常温下,向10 mL 0.01 mol·L-1 H2C2O4溶液中滴加10 mL 0.01 mol·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ;
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为 ______________mol·L-1。
(5)以二甲醚(CH3OCH3)、空气、H2SO4为原料,铂为电极可构成燃料电池,其工作原理与甲烷燃料电池的原理相似。请写出该电池负极上的电极反应式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com