
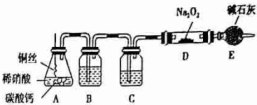
分析 探究NO与过氧化钠的反应,实验设计装置中:装置A产生NO时,要除尽装置中的空气,用碳酸钙和稀硝酸反应生成二氧化碳气体用来排净装置中空气,排尽装置中的二氧化碳,防止二氧化碳与过氧化钠反应需要装置B中的氢氧化钠溶液吸收二氧化碳气体,铜丝和稀硝酸反应后生成一氧化氮气体,装置D必须干燥,防止水与过氧化钠反应,需要装置C中的浓硫酸吸收水蒸气,采取措施装置E防止空气进入装置,
(1)装置A产生NO时,为避免空气中的氧气和一氧化氮反应要除尽装置中的空气,用碳酸钙和稀硝酸反应生成二氧化碳气体用来排净装置中空气;
(2)排尽装置中的二氧化碳,防止二氧化碳与过氧化钠反应需要装置B中的氢氧化钠溶液吸收二氧化碳气体,铜丝和稀硝酸反应后生成一氧化氮气体,装置D必须干燥,防止水与过氧化钠反应,需要装置C中的浓硫酸吸收水蒸气,采取措施装置E防止空气进入装置,
(3)若Na2O2已反应完全,D中固体产物溶于水,溶液显强碱性说明含有Na2O,向溶液中加入酸性KMnO4溶液,紫色退去,说明存在还原性物质,即可能有NaNO2,
(4)D中白色固体产物密闭加热部分变为淡黄色,说明其中还有NaNO3,2NaNO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNO2+O2↑、生成的O2再次把Na2O氧化为Na2O2而显淡黄色,由此可知Na2O2与NO反应的产物有NaNO3、NaNO2和Na2O.
解答 解:探究NO与过氧化钠的反应,实验设计装置中:装置A产生NO时,要除尽装置中的空气,用碳酸钙和稀硝酸反应生成二氧化碳气体用来排净装置中空气,排尽装置中的二氧化碳,防止二氧化碳与过氧化钠反应需要装置B中的氢氧化钠溶液吸收二氧化碳气体,铜丝和稀硝酸反应后生成一氧化氮气体,装置D必须干燥,防止水与过氧化钠反应,需要装置C中的浓硫酸吸收水蒸气,采取措施装置E防止空气进入装置,
(1)装置A产生NO时,为避免空气中的氧气和一氧化氮反应要除尽装置中的空气,用碳酸钙和稀硝酸反应生成二氧化碳气体用来排净装置中空气,A装置中放入碳酸钙的目的是使碳酸钙与稀硝酸反应生成CO2,排除装置中的空气,
故答案为:使碳酸钙与稀硝酸反应生成CO2,排除装置中的空气;
(2)排尽装置中的二氧化碳,防止二氧化碳与过氧化钠反应需要装置B中的氢氧化钠溶液吸收二氧化碳气体,铜丝和稀硝酸反应后生成一氧化氮气体,装置D必须干燥,防止水与过氧化钠反应,需要装置C中的浓硫酸吸收水蒸气,采取措施装置E防止空气进入装置,装置B、C中的试剂分别是氢氧化钠溶液、浓硫酸溶液,E 的作用是防止空气中的CO2、水蒸气进入装置D中,干扰产物的判断,
故答案为:氢氧化钠溶液;浓硫酸;防止空气中的CO2、水蒸气进入装置D中,干扰产物的判断;
(3)若Na2O2已反应完全,D中固体产物溶于水,溶液显强碱性说明含有Na2O,向溶液中加入酸性KMnO4溶液,紫色退去,说明存在还原性物质,即可能有NaNO2,由此现象推断固体产物中可能含有的物质是:Na2O、NaNO2,
故答案为:Na2O、NaNO2;
(4)D中白色固体产物密闭加热部分变为淡黄色,说明其中还有NaNO3,2NaNO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaNO2+O2↑、生成的O2再次把Na2O氧化为Na2O2而显淡黄色,由此可知Na2O2与NO反应的产物有NaNO3、NaNO2和Na2O,其反应的化学方程式为:2Na2O2+2NO=NaNO3+NaNO2+Na2O
故答案为:NaNO3;2Na2O2+2NO=NaNO3+NaNO2+Na2O.
点评 本题考查了物质性质、物质制备、物质反应现象、除杂和避免干扰实验的操作等知识点,掌握基础是解题关键,题目难度中等.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
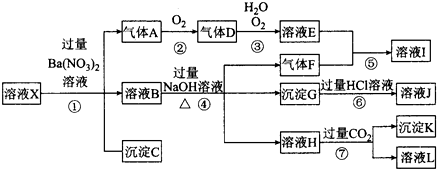
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
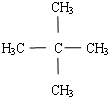 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙炔和苯 | B. | 甲烷和乙烷 | C. | 乙烯和丁炔 | D. | 苯和苯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ①②⑤⑦⑧ | C. | ①②③ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
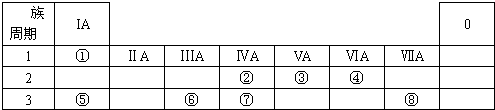
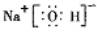 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑥⑦ | B. | ①②④⑦ | C. | ②③④⑥ | D. | ②③⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
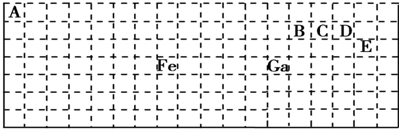
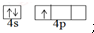 .
.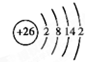
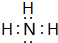 ,含有共价键化学键,E的电子表达式是
,含有共价键化学键,E的电子表达式是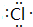 .
.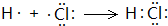 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com