
分析 N、P元素是植物生成的重要的营养元素;水体富营养化会使植物大量繁殖,消耗水中的氧气,据此分析.
解答 解:N、P元素是植物生成的重要的营养元素,当过量使用含氮、磷元素的化肥或大量使用含磷的洗涤剂等化学产品,加上一些生活污水处理不当,容易使其中的氮、磷元素随着水流进入各种水体,导致水中藻类大量繁殖;水体富营养化会使植物大量繁殖,消耗水中的氧气;从而使水体中的动物会因为缺少氧气而大量死亡,致死的动植物遗骸在水底沉积腐烂,使水质不断恶化,并能通过食物链危害人体健康;
故答案为:N;P;氧;动物;沉积腐烂;食物链.
点评 本题考查了水资源的污染,题目难度不大,注意把握水体富营养化的原因以及危害,侧重于考查学生对化学知识的应用能力.


科目:高中化学 来源: 题型:解答题
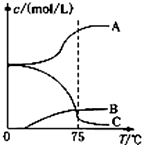 氯酸钠(NaClO3)是无机盐工业的重要产品之一.
氯酸钠(NaClO3)是无机盐工业的重要产品之一.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 名称 | 性状 | 密度 | 溶点℃ | 沸点℃ | 溶解度 | |
| 水 | 乙醚 | |||||
| 环已醇 | 无色,有刺激性气味 | 0.9624 | 25.93 | 161.5 | 5.67g/100mL | ∞ |
| 环已酮 | 无色,有刺激性气味 | 0.9478 | - | 155.7 | 2.4g/100mL | ∞ |
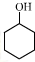 +1 Na2Cr2O7+4H2SO4→3
+1 Na2Cr2O7+4H2SO4→3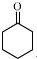 +1 Na2SO4+1 Cr2(SO4)3+7 H2O
+1 Na2SO4+1 Cr2(SO4)3+7 H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
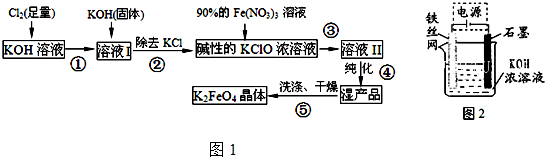
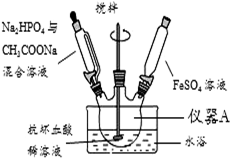 磷酸亚铁[Fe3(PO4)2•8H2O]为白蓝色晶体,溶于强酸,不溶于水、醋酸和乙醇.主要用于制造磷酸铁锂电池.实验室制备磷酸亚铁的装置示意图如图、反应和实验步骤如下.
磷酸亚铁[Fe3(PO4)2•8H2O]为白蓝色晶体,溶于强酸,不溶于水、醋酸和乙醇.主要用于制造磷酸铁锂电池.实验室制备磷酸亚铁的装置示意图如图、反应和实验步骤如下.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其它分散系的本质特征是:胶体粒子直径在1-100nm之间 | |
| B. | 一定温度、压强下,气体体积由其分子的大小决定 | |
| C. | 氧化还原反应的本质是电子转移 | |
| D. | 在1L2mol/L的氢氧化铁胶体中含有氢氧化铁胶粒数小于2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com