
可逆反应N2+3H22NH3是工业上合成氨的重要反应。
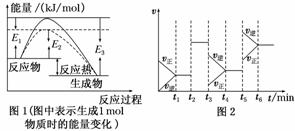
(1)根据图1请写出合成氨的热化学方程式
________________________________________________________________________
________________________________________________________________________
(热量用E1、E2或E3表示)。
(2)图1中虚线部分是通过改变化学反应中的________条件,该条件的改变与图2中哪一时刻条件的改变相同________(用“t1……t6”表示)。
(3)图2中t3时刻改变的条件是________________,t5时刻改变的条件是________________。
科目:高中化学 来源: 题型:
下列说法不正确的是
A.CO2和CH4都是温室气体 B.SO2、NO2都是形成酸雨的气体
C.汽油、花生油的主要成分都是油脂 D.毛发和蚕丝的主要成分都是蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中,书写正确的是 ( )
A . 弱酸酸式盐NaHB在水溶液中水解:HB–+H2O H3O++B2–
H3O++B2–
B . 电解饱和食盐水:C1-+2H2O H2↑+Cl2↑+OH-
H2↑+Cl2↑+OH-
C . 氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e一=4OH-
D . FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
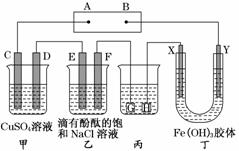
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。
请回答:
(1)B极是电源的______________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明_____________________________,
在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________。
(3)现用丙装置给铜件镀银,则H应是______________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时 (此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
T0℃时,在2 L的密闭容器中发生反应:X(g)+Y(g)Z(g)(未配平),各物质的物质的量随时间变化的关系如图a所示。其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示。下列叙述正确的是( )
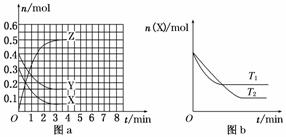
A.该反应的正反应是吸热反应
B.T0℃,从反应开始到平衡时:v(X)=0.083 mol·L-1·min-1
C.图a中反应达到平衡时,Y的转化率为37.5%
D.T1℃时,若该反应的平衡常数K=50,则T1<T0
查看答案和解析>>
科目:高中化学 来源: 题型:
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项错误的是( )
①2CN-+H2O+CO2===2HCN+CO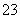
②2HCOOH+CO ===2HCOO-+H2O+CO2↑
===2HCOO-+H2O+CO2↑
③中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
④等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
在科学史上中国有许多重大的发明和发现,为世界现代物质文明奠定了基础.以下发明或发现属于化学史上中国对世界重大贡献的是()
①造纸 ②印刷技术 ③火药④指南针 ⑤炼铜、炼铁、炼钢 ⑥合成有机高分子材料 ⑦人工合成牛胰岛素 ⑧提出原子﹣﹣分子论学说.
| A. | ①②③④⑧ | B. | ①③⑤⑦ | C. | ②④⑥ | D. | ⑤⑥⑦⑧2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在20℃时一刚性容器内部有一不漏气且可滑动的活塞将容器分隔成左、右室两室.左室充入N2,右室充入H2和O2,活塞正好停留离左端1/5处(如图a)然后点燃引爆H2和O2混合器,活塞先左弹(设容器不漏气),恢复至原来温度,活塞恰好停在中间(如图b),水蒸气的体积可忽略,则反应前H2和O2的体积比可能是()
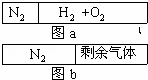
| A. | 7:1 | B. | 1:3 | C. | 1:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据表中信息,判断以下叙述正确的是
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的稳定性为H2T<H2R B.单质与稀盐酸反应的剧烈程度为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com