
 某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.
某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案.分析 (2)为了检验CO2的生成,应利用明显的现象来说明,二氧化碳为酸性氧化物;
(3)只有在加热NaHCO3时,试管B中才有气泡产生,可知分解生成二氧化碳,而碳酸钠不分解;
(4)加热后的A试管中仍留有少量白色固体为碳酸钠,溶于水后水解显碱性;
(5)n(NaHCO3)=$\frac{16.8g}{84g/mol}$=0.2mol,结合2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O及V=nVm计算.
解答 解:(2)若生成二氧化碳,紫色石蕊溶液变红,而二氧化碳与KOH溶液反应现象不明显,则检验气体的生成B中为紫色石蕊溶液,故答案为:紫色石蕊溶液;
(3)只有在加热NaHCO3时,试管B中才有气泡产生,可知分解生成二氧化碳,管B中才有气泡产生且有红色出现,而碳酸钠不分解,可知稳定性为Na2CO3 >NaHCO3,
故答案为:红色;>;
(4)加热后的A试管中仍留有少量白色固体为碳酸钠,溶于水后水解显碱性,再滴加1~2滴酚酞试液,可观察到的现象是溶液呈红色,故答案为:溶液呈红色;
(5)n(NaHCO3)=$\frac{16.8g}{84g/mol}$=0.2mol,由2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O可知,生成气体的物质的量为0.1mol,理论上可产生CO2气体的体积V=nVm=0.1mol×22.4L/mol=2.24L,故答案为:2.24.
点评 本题考查碳酸钠、碳酸氢钠的性质比较,为高频考点,把握碳酸钠、碳酸氢钠的热稳定性大小及发生的反应为解答的关键,侧重分析、实验及计算能力的考查,题目难度不大.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:选择题
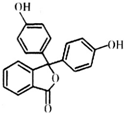 酚酞医药名为果桃,可治疗消化系统疾病,其有效成分的结构简式如图所示.下列对该有效成分的说法正确的是( )
酚酞医药名为果桃,可治疗消化系统疾病,其有效成分的结构简式如图所示.下列对该有效成分的说法正确的是( )| A. | 所有原子可能共平面 | |
| B. | 能发生加聚反应生成高分子化合物 | |
| C. | 酚酞的水解产物中含有醇羟基 | |
| D. | 1 mol该物质最多能与含4 mol NaOH的烧碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

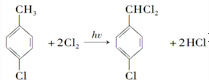 ;该反应的类型为取代反应.
;该反应的类型为取代反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 前四周期原子序数依次增大的六种元素A,B,D,X,Y,Z,基态时核外电子排布具有以下特征:A的电子层数和最外层电子数相等,非金属元素B的已成对电子数是未成对电子数的2倍,且A和B位于不同周期;D和X的价电子层中未成对电子均只有1个,并且D-和X+的电子相差为8;Y、Z与X位于同一周期,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.回答下列问题:
前四周期原子序数依次增大的六种元素A,B,D,X,Y,Z,基态时核外电子排布具有以下特征:A的电子层数和最外层电子数相等,非金属元素B的已成对电子数是未成对电子数的2倍,且A和B位于不同周期;D和X的价电子层中未成对电子均只有1个,并且D-和X+的电子相差为8;Y、Z与X位于同一周期,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)═CaWO4(s)+2OH-(aq).
已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)═CaWO4(s)+2OH-(aq).| 温度/℃ | 25 | 50 | 90 | 100 |
| K | 79.96 | 208.06 | 222.88 | 258.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 芳香族化合物A(C8H6O4)能与NaHCO3溶液反应生成CO2.由A与对二氯苯(
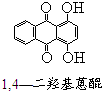
芳香族化合物A(C8H6O4)能与NaHCO3溶液反应生成CO2.由A与对二氯苯( )为原料经多步反应可合成1,4-二羟基蒽醌(结构如图所示).
)为原料经多步反应可合成1,4-二羟基蒽醌(结构如图所示). .
.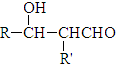 $\stackrel{△}{→}$
$\stackrel{△}{→}$
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com