
【题目】下列符号不符合事实的是 ( )
A. 4s2 B. 2p3 C. 3d8 D. 3f14
科目:高中化学 来源: 题型:
【题目】下列关于有机物说法正确的是
A. C7H8与C6H6互为同系物
B. 由乙酸与乙醇制备乙酸乙酯的反位属于加成反位
C. C3H6Br2有4种同分异构体
D. 油脂在人体内最终分解为甘油和高级脂肪酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用固体硫酸亚铁制取颜料铁红,反应原理是:2FeSO4 ![]() Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
A.(I)中会生成 BaSO3、BaSO4两种沉淀
B.可将(I)中的 BaCl2溶液改为 Ba(NO3)2溶液
C.(II)所盛 x 应为品红溶液
D.(III)的作用是检验生成的SO2 气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种物质相互反应时,无论哪种过量,都可用同一个离子方程式表示的有( )
①碳酸钠溶液与盐酸 ②偏铝酸钠溶液与盐酸
③硫酸铝溶液与氨水 ④碳酸氢钙溶液与澄清石灰水
⑤碘化亚铁溶液与氯水 ⑥硝酸银溶液与氨水
⑦苯酚钠溶液与二氧化碳 ⑧铁与稀硝酸
A.3个 B.4个 C.5个 D.6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为A g
②称量装有试样的坩埚质量为B g ③加热
④冷却⑤称量坩埚和残余物的质量为C g
⑥重复③至⑤操作,直至恒重,质量为D g
(1)坩埚中发生反应的化学方程式为__________________。
(2)计算Na2CO3质量分数必须用到的测定数据为___________(填“A”、“B”、“C”或“D”)。
乙方案:
在天平上准确称取0.3000 g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000 mo1·L-1,的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为NaHCO3。重复上述操作两次,消耗盐酸的体积为20.00 mL。
(3)配制上述盐酸标准溶液100 mL,若用2.0 mol·L-1HCl进行配制,需用滴定管量取该HCl溶液________mL;定容时俯视刻度线,将导致配制的溶液浓度___________(填“偏高”、“偏低”或“没有影响”)。
(4)样品中Na2CO3的质量分数为___________(用百分数表示,精确到0.1%)。
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
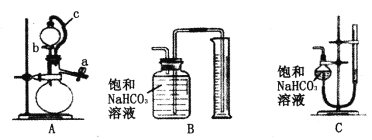
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若装置不漏气,则观察到的现象为__________________。实验时,装置A中c的作用_____________、_____________。
(6)为了提高测定的准确性,应选用装置A和__________(填写字母标号)进行实验。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)==CO2(g) △H1<0①
途径II:先制成水煤气:C(s)+H2O(g)==CO(g)+H2(g) △H2>0②
再燃烧水煤气:2CO(g)+O2(g)==2CO2(g) △H3<0③
2H2(g)+O2(g)==2H2O(g) △H4<0④
请回答下列问题:
(1)途径I放出的热量 ( 填“大于”“等于”或“小于”) 途径II放出的热量。
(2)△H1、△H2、△H3、△H4的数学关系式是 。
(3)12g 炭粉在氧气中不完全燃烧生成一氧化碳,放出110.35kJ热量。其热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列十种物质:①O2;②Fe;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁胶体;⑧硫酸钠溶液;⑨稀硝酸;⑩Cu2(OH)2CO3。
(1)按物质的树状分类法填写表格的空白处:
分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 |
属于该类的物质 | ② | ⑧⑨ |
(2)上述物质中属于非电解质的有_________;上述物质中能与盐酸反应的电解质有________(填序号)。
Ⅱ.(1)在 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O 的反应中,氧化剂是_________,还原产物是_________,氧化产物与还原产物的质量比是_________。
(2)在反应MnO2+4HCl=MnCl2+Cl2↑+2H2O中,每生成标准状况下4.48LCl2,转移的电子的物质的量为___________mol。
Ⅲ.Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程,据此回答下列问题:
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ _________+ ________![]() _________+ ________+H2O
_________+ ________+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某阳离子为钠离子的溶液中,可能含有SO42-、CO32-、Cl-的一种或几种,只取原溶液一次,便能一一检验其中存在的阴离子。下列加入试剂的顺序最合理的是
A. HNO3、Ba(NO3)2、AgNO3 B. Ba(NO3)2、AgNO3、HNO3
C. 酚酞、Ba(NO3)2、AgNO3 D. HCl、BaCl2、AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现往1L的容器中通入CO2、H2各2mol。在一定条件下让其发生反应:CO2+H2![]() CO+H2O,回答下列问题:
CO+H2O,回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的浓度为1mol·L-1。该条件下平衡常数K1=________。
(2)在(1)基础上,把体系的温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知平衡时c(H2O)=______________(保留2位有效数字)。
(3)该可逆反应的正反应为________反应(填“吸热”或“放热”)。
(4)在(1)基础上,压缩容器体积至0.5L。该条件下的平衡常数为K3。则K3________(填“大于”、“等于”或“小于”)K1,理由是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com