
 ��صķ�����Ӧ���ǻ�ѧ���Ƕ�����������Ҫ����֮һ��
��صķ�����Ӧ���ǻ�ѧ���Ƕ�����������Ҫ����֮һ������ ��1������ȼ�ϵ�صķ�Ӧԭ����ȼ��ȼ�յ�������ԭ��Ӧ��ȼ���ڸ����Ϸ���������Ӧ������������������ԭ��Ӧ����ϵ���ʻ�����д�缫��Ӧ��
��2����ʯī�缫��ⱥ��ʳ��ˮ����ʼ���������������ӷŵ磬��Һ�ʼ���ʹ��̪��죻���ݼ״�ȼ�ϵ�صķ�Ӧ����ϵ�ص�����Ч�ʣ����õ���ת�ƽ��м��㣻
��1������ת�Ƶķ��������Ÿ����ܵķ����ƶ���ͨ��Ksp�Ĵ�С��֪�������ʸ������ܣ�
��2����Cr2O72-�����Թ�ҵ��ˮ�м�������������Ӧ���������ӣ����۸����Ӻ�ˮ������ԭ���غ�͵���غ���ƽ��д���ӷ���ʽ��
�������ܶȻ�������������������Ũ�Ƚ�����ӻ���������������Ũ�ȵõ���ҺpH��
���������ӷ���ʽ������ϵ����õ���
��� �⣺��1������װ�ÿ���֪��d�����ɴ�����ˮ������e�缫��ͨ�����������Ӧ������������Һ�������缫��ӦΪ��O2+4e-+4H+=2H2O��
�ʴ�Ϊ��O2+4e-+4H+=2H2O��
��2����ʯī�缫��ⱥ��ʳ��ˮ����ʼ���������������ӷŵ磬��Һ�ʼ���ʹ��̪��죻��6.4g�״���ȫ��Ӧ����CO2ʱ�����ݷ�Ӧ2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g���������ļ״�2molʱ��ת�Ƶ���Ϊ12mol�����Ե�6.4g�״���0.2mol�״���ȫ��Ӧ����CO2ʱ��ת�Ƶ�����1.2mol����ص�����Ч��Ϊ80%�������·ͨ���ĵ��Ӹ���=1.2mol��80%��6.02��1023=5.8��1023��
�ʴ�Ϊ��������5.8��1023��
��1������Ksp��FeS����Ksp��CuS������������ͬ������CuS���ܽ�ȸ�С����������������CuS�ķ�����У������ӷ���ʽΪFeS��s��+Cu2+��aq��=CuS��s��+Fe2+��aq�����ʴ�Ϊ��FeS��s��+Cu2+��aq��=CuS��s��+Fe2+��aq����
��2���ٹ�ҵ��Ϊ�˴�������Cr2O72-�����Թ�ҵ��ˮ�����̷���FeSO4•7H2O���ѷ�ˮ�е����۸����ӻ�ԭ�����۸����ӣ�Cr2O72-�����Թ�ҵ��ˮ�м�������������Ӧ���������ӣ����۸����Ӻ�ˮ����Ӧ�����ӷ���ʽΪ��Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O��
�ʴ�Ϊ��Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O��
�ڳ����£�Cr3+������ȫŨ��С��10-5mol/L��Cr��OH��3���ܶȻ�Ksp=1��10-32=c��Cr3+��c3��OH-����c3��OH-��=$\frac{1��1{0}^{-32}}{1��1{0}^{-5}}$=10-27��c��OH-��=1��10-9mol/L���������ӻ�Kw=c��H+��c��OH-����c��H+��=$\frac{1{0}^{-14}}{1{0}^{-9}}$=10-5��mol/L������ҺpH=5��
�ʴ�Ϊ��5��
������������������100m3������+6�ۣ�78mg•L-1�ķ�ˮ����Ԫ�����ʵ���=$\frac{100000L��78��1{0}^{-3}g/L}{52g/mol}$=150mol��Cr2O72-���ʵ���75mol����
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
1 6
75mol 450mol
�����̷�������=450mol��278g/mol=125100g=125.1kg��
�ʴ�Ϊ��125.1��
���� ���⿼�����ܶȻ�����Ӱ�����غͼ���Ӧ�ã�����ת����ϵ�ķ���Ӧ�ã����ӷ���ʽ���㷽�������ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Լ��Դ�������Դ������ | |
| B�� | �������ɻ�ʯԭ�ϣ�������������Դ��Ҫ�� | |
| C�� | ����ֱ����ʹ�öԴ������������ƻ����õķ����� | |
| D�� | ���á���ɫ��ѧ�����գ�ʹԭ�Ͼ�����ת��Ϊ����Ҫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�28g CO�к��еķ�����ΪNA | |
| B�� | 1.0 mol•L-1 Na2SO4��Һ��������Na+��Ϊ2NA | |
| C�� | ��״���£�22.4 L HCl������������ԭ����ΪNA | |
| D�� | 1 mol N2�����е�ԭ����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֬�ڿ�������ȫȼ��ת��Ϊˮ�Ͷ�����̼ | |
| B�� | ���ǡ���ѿ�ǵķ���ʽ����C12H22O11������Ϊͬ���칹�� | |
| C�� | ����ʳƷ��װ��������Ʒ���������������ϣ��ɻ��������� | |
| D�� | ������ϩ����ǿ�ȴ���ʴ��ǿ������������װ�賤ʱ�䱣���ʳƷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
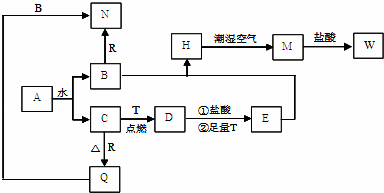
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ���õ�ΰ�̽�����������ʣ�ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ����������������ס������ΰ壮���ж�ʵ������Ľ�����ȷ���ǣ�������
��ͼ���õ�ΰ�̽�����������ʣ�ʵ��ʱ��NaOH�����ϵμ���Ũ��ˮ����������������ס������ΰ壮���ж�ʵ������Ľ�����ȷ���ǣ�������| ѡ�� | ʵ������ | ���� |
| A | ��ɫʯ����ֽ���� | NH3��������ˮ |
| B | Ũ���ḽ���ް��� | NH3��Ũ���������Ӧ |
| C | �Ȼ�����Һ����� | NH3��AlCl3��Һ��Ӧ��Al3++3OH-��Al��OH��3�� |
| D | Ũ���ḽ���а��� | NH3��ӷ�����HCl��Ӧ��NH3+HCl��NH4Cl |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
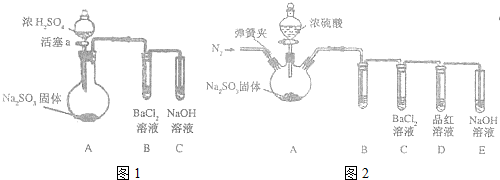
�鿴�𰸺ͽ���>>
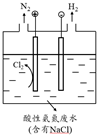
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ���в������ݣ����в��������� | |
| B�� | �ٺ͢��ж����������� | |
| C�� | �ٺ͢��ж��������ݣ�������H2��������O2 | |
| D�� | �ٺ͢��ж��������ݣ��Ҷ���H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
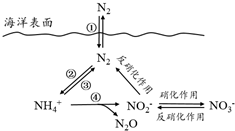 ��Ԫ���ں����е�ѭ����������������̬ϵͳ�Ļ����ؼ���������������ѭ�����̿�����ͼ��ʾ��
��Ԫ���ں����е�ѭ����������������̬ϵͳ�Ļ����ؼ���������������ѭ�����̿�����ͼ��ʾ��| �¶�/�� | ������������/mg | ����24h | ����48h |
| ��������/mg | ��������/mg | ||
| 20 | 1008 | 838 | 788 |
| 25 | 1008 | 757 | 468 |
| 30 | 1008 | 798 | 600 |
| 40 | 1008 | 977 | 910 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com