


分析 (1)a仪器的名称为分液漏斗;发生反应的玻璃仪器名称为圆底烧瓶;装置I中浓硫酸与亚硫酸钠反应产生二氧化硫气体,同时生成硫酸钠和水;
(2)处理过量的SO2尾气,既要吸收SO2尾气,同时能防倒吸;
(3)次氯酸具有强氧化性,能氧化亚硫酸氢根离子为硫酸;
(4)Na2S2O5晶体在空气中易被氧化为Na2SO4,用盐酸、氯化钡溶液检验样品中是否含有硫酸根即可;
(5)①碘单质滴定,滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI,所以滴定终点为溶液变化为蓝色且半分钟不褪色,
令100mL葡萄酒中二氧化硫的质量为mg,则:
SO2+2H2O+I2═H2SO4+2HI
64g 1mol
mg 0.1L×0.01mol/L
所以,64g:mg=1mol:0.1L×0.01mol/L,
解得m=6.4g
计算得到该次实验测得样品中抗氧化剂的残留量(以游离SO2计算);
②若有部分HI被空气氧化,则消耗碘的量偏小,故测定二氧化硫的量偏小.
解答 解:(1)a仪器的名称为分液漏斗,发生反应的玻璃仪器名称为圆底烧瓶;装置I中浓硫酸与亚硫酸钠反应产生二氧化硫气体,同时生成硫酸钠和水,化学方程式:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,
故答案为:分液漏斗;圆底烧瓶;Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)处理过量的SO2尾气,a项装置瓶口封闭,错误;b项食盐水不能将大量的SO2尾气吸收,错误;c项漏斗口没入了液体中,错误,d项氢氧化钠溶液可吸收SO2尾气,同时能防倒吸,正确;
故答案为:d;
(3)次氯酸具有强氧化性,能氧化亚硫酸氢根离子为硫酸,反应的离子方程式HSO3-+HClO=SO42-+Cl-+2 H+,
故答案为:HSO3-+HClO=SO42-+Cl-+2 H+;
(4)Na2S2O5中S元素的化合价为+4价,因此会被氧化为为+6价,即晶体在空气中易被氧化为Na2SO4,用盐酸、氯化钡溶液检验样品中是否含有硫酸根即可,实验方案为:取少量Na2S2O5晶体于试管中,加入适量水溶解,滴加盐酸,振荡,再滴加氯化钡溶液,有白色沉淀生成,
故答案为:取少量焦亚硫酸钠晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成;
(5)①碘单质滴定,滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI,所以滴定终点为溶液变化为蓝色且半分钟不褪色,
令100mL葡萄酒中二氧化硫的质量为mg,则:
SO2+2H2O+I2═H2SO4+2HI
64g 1mol
mg 0.1L×0.01mol/L
所以,64g:mg=1mol:0.1L×0.01mol/L,
解得m=6.4g
故该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为$\frac{6.4g}{0.1L}$=0.64 g/L
故答案为:当滴入最后一滴标准液时,溶液显蓝色,且半分钟不退色;0.64;
②若有部分HI被空气氧化,则消耗碘的量偏小,故测定二氧化硫的量偏小,则测定结果偏低,故答案为:偏低.
点评 本题考查SO2的制取,Na2S2O5含量的测定,实验操作等基础知识,难度中等,掌握实验原理是解题的关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ④<①<③<② | B. | ①<④<③<② | C. | ①<②<③<④ | D. | ④<③<①<② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 125g CuSO4•5H2O晶体中含有Cu2+离子数一定小于0.5NA | |
| B. | 常温下,pH=3的醋酸溶液中,醋酸分子的数目一定大于10-3NA | |
| C. | 由S6、S7、S8组成的硫蒸气6.4g,其中所含硫原子数一定为0.2NA | |
| D. | 3.6g C与3.36L O2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式为: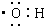 | |
| B. | 甘氨酸的结构简式为:C2H5NO2 | |
| C. | 间羟基苯甲酸的结构简式为: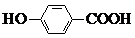 | |
| D. | Na2S在溶液中水解的离子方程式为:S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

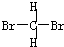 和
和 E.甲烷和庚烷F.
E.甲烷和庚烷F.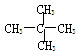 和C(CH)3
和C(CH)3 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能发生加成反应 | |
| B. | 乙醇和乙酸都能与氢氧化钠溶液反应 | |
| C. | 乙烯和苯都能使酸性KMnO4溶液褪色 | |
| D. | 葡萄糖和蔗糖都可发生银镜反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com