
分析 (1)根据操作步骤选取实验仪器;
(2)根据溶液稀释前后溶质的物质的量不变计算所需浓硫酸溶液的体积;根据浓硫酸的体积选取量筒,注意所选量筒的容积应稍大于或等于量取溶液的体积;
(3)根据c=$\frac{n}{V}$分析操作对溶质的物质的量或对溶液的体积的影响判断.
解答 解:(1)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸溶液在烧杯中稀释,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有玻璃棒、量筒、胶头滴管、小烧杯、500ml容量瓶,所以用不到的仪器有烧瓶、托盘天平、药匙,还缺少的仪器:500mL容量瓶;
故答案为:②⑥⑦;500mL容量瓶;
(2)设需要浓硫酸体积为V,则根据溶液稀释前后溶质的物质的量不变计算得:0.24mol/L×0.5L=18.4mol/L×V,V=0.0054L=6.5mL;
量筒的容积应稍大于或等于量取溶液的体积,所以应选择10mL量筒;
故答案为:6.5;10;
(3)根据c=$\frac{n}{V}$可知,凡是n偏大或者使V偏小的操作都会使溶液的浓度偏高,例如:加水定容时腐蚀刻度线、未冷却到室温定容,都会使溶液体积偏小,溶液浓度偏高;
故答案为:加水定容时腐蚀刻度线、未冷却到室温定容.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意误差分析的方法和技巧.


科目:高中化学 来源: 题型:选择题
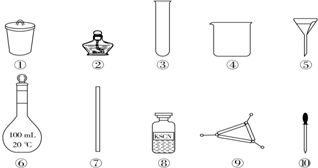
| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用⑥和⑦ | |
| C. | 过滤得到滤液,选用④、⑤和⑦ | |
| D. | 检验滤液中的Fe3+,选用③、⑧和⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Cl-、CO32- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | Ba2+、Cu2+、SO42-、Cl- | D. | NH4+、Mg2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用等量锌粒代替锌粉 | B. | 改用100 mL 0.5 mol/L盐酸 | ||
| C. | 多用300 mL 1 mol/L盐酸 | D. | 适当升高温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com