
| A、5mol | ||
| B、3mol | ||
C、
| ||
D、
|
| 2b |
| 3 |
| 5 |
| 3 |


科目:高中化学 来源: 题型:
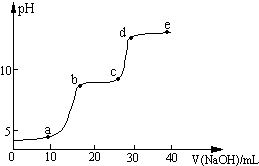 某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.在0.1mol?L-1 MgSO4、0.05mol?L-1 Al2(SO4)3的混合溶液中滴加0.5mol?L-1 NaOH溶液,借助氢离子传感器和相应分析软件,测得溶液的pH随NaOH溶液的加入变化情况如图所示.
某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.在0.1mol?L-1 MgSO4、0.05mol?L-1 Al2(SO4)3的混合溶液中滴加0.5mol?L-1 NaOH溶液,借助氢离子传感器和相应分析软件,测得溶液的pH随NaOH溶液的加入变化情况如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠钾合金能用作原子反应堆的导热剂是由于二者是活泼金属易失电子 |
| B、用饱和碳酸氢钠制造灭火剂比用饱和碳酸钠制造灭火剂的效果好 |
| C、碳酸钠可用于制造洗涤剂,因为碳酸钠是碱 |
| D、五彩缤纷的焰火是K单质燃烧所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| A、①② | B、①③ | C、①④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al(OH)3沉淀 |
| B、只有[Al(OH)4]- |
| C、Al(OH)3沉淀和Al3+ |
| D、Al(OH)3沉淀和[Al(OH)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③ |
| C、④⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
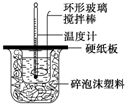 某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL1.0mol/L盐酸跟50mL1.1mol/L 氢氧化钠溶液在如图装置中进行中和反应.在大烧杯底部垫碎泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、I -、NO3-、Cl - |
| B、Cu2+、Na+、NO3-、SO42- |
| C、Ag+、Fe3+、Cl-、SO42- |
| D、NH4+、OH-、Cl-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com