
分析 (1)“1.5g碳酸钙与600mg的钙”的计量关系实际上是指1.5g碳酸钙含有600mg的钙,根据化合物中元素的质量分数的计算公式找关系;
(2)①为了测定片剂中碳酸钙的含量,经过了多步反应,可得关系式:2KMnO4~5H2C2O4~5CaCO3,据此计算;
②计算每片中Ca元素的质量,根据Ca元素含量进行命名.
解答 解:(1)1.5g碳酸钙含有钙元素的质量是:1.5g×$\frac{40}{100}$=0.6g=600mg,答:“1.5g碳酸钙与600mg的钙”的计量关系是1.5g×$\frac{40}{100}$=0.6g=600mg;故答案为:600;
(2)设10片药片中含CaCO3的质量为m
2KMnO4 ~5H2C2O4 ~5CaCO3
2mol 500g
0.012L×0.05mol/L×$\frac{1000ml}{20ml}$ m
所以2mol:0.012L×0.05mol/L×$\frac{1000ml}{20ml}$=500g:m
解得m=7.5g
所以,每片中碳酸钙的含量是$\frac{7.5g}{10}$=0.75g
故答案为:每片中碳酸钙的含量是0.75g;
②每片中钙元素的含量为0.75g×$\frac{40}{100}$=0.3g,故应钙尔奇D300片剂,
故答案为:300.
点评 本题考查化学方程的计算,难度中等,题目涉及多步反应,注意利用关系式进行计算.


科目:高中化学 来源: 题型:解答题
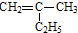 的键线式是
的键线式是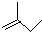
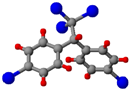 所示.请写出其结构简式
所示.请写出其结构简式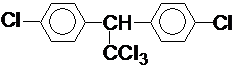
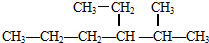 进行命名,它的名称是2-甲基-3-乙基已烷
进行命名,它的名称是2-甲基-3-乙基已烷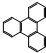 的一氯取代物有2 种.
的一氯取代物有2 种.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人类历史上使用最早的合金是青铜 | |
| B. | 金属钛有可能在21世纪得到广泛运用 | |
| C. | 广泛运用铝合金,是因为铝不能与酸、碱、O2等反应 | |
| D. | 目前世界上用途最广的合金是钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
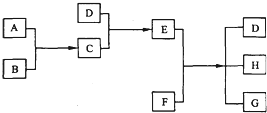
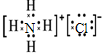
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com