
| A. | n+1 | B. | n+2 | C. | n+3 | D. | n+5 |
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:选择题
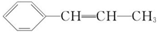
| A. | 该物质属于苯的同系物 | |
| B. | 1 mol 该物质一定条件下最多能与 1 mol H2 发生加成反应 | |
| C. | 所有碳原子可能在同一平面上 | |
| D. | 所有原子可能都在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙和盐酸反应:CO32-+2H-═H2O+CO↑ | |
| B. | 将Fe2O3溶于稀盐酸中:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 向稀盐酸溶液中加入铁粉:3Fe+6H-═3Fe3++3H2↑ | |
| D. | 把少量钠投人水中:Na+H2O═OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
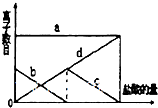 向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化.四条曲线与溶液中离子的对应关系,正确的是( )
向一定量的K2CO3溶液中缓慢地滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中离子数目也相应地发生如图变化.四条曲线与溶液中离子的对应关系,正确的是( )| A. | a:Cl- b:K+ c:$C{{O}_{3}}^{2-}$ d:$HC{{O}_{3}}^{-}$ | |
| B. | a:Cl- b:$C{{O}_{3}}^{2-}$ c:K+ d:$HC{{O}_{3}}^{-}$ | |
| C. | a:K+ b:$C{{O}_{3}}^{2-}$ c:$HC{{O}_{3}}^{-}$ d:Cl- | |
| D. | a:K+ b:$HC{{O}_{3}}^{-}$ c:Cl- d:$C{{O}_{3}}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
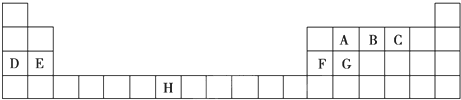
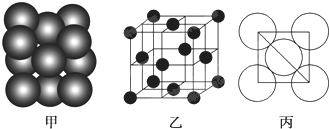
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com