
����Ŀ��A��B��C��X��Ϊ��ѧ�����Ĵ��������֮��������ת����ϵ����Ӧ����������������ȥ����
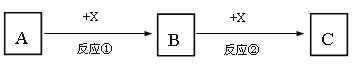
��1����A��B��C��Ϊ����ͬ�ַǽ���Ԫ�صĻ����AΪʹʪ��ĺ�ɫʯ����ֽ���������壬B�Ӵ��������̱�ΪC����Ӧ���Ļ�ѧ����ʽΪ_______________________��
��2����A��B��CΪ��ɫ��Ӧ���ʻ�ɫ�Ļ����XΪ��ɫ��ζ���壬��Ӧ�������ӷ���ʽΪ_____________________________________________��
��3����A��B��C��Ϊ����ͬ�ֽ���Ԫ�صĻ����X��ǿ���Ӧ�������ӷ���ʽΪ________________________________________________��
��4����AΪ����Fe��XΪϡ���ᣬ��Ӧ�������ӷ���ʽΪ___________________������B����Һ�м�������������Һ������Ϊ________________________________________����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��5����A��X��Ϊ���ʣ�BΪ��ʹƷ����Һ��ɫ�����壬��Ӧ���Ļ�ѧ����ʽΪ___________________________��
���𰸡� ![]() CO32- + CO2 + H2O �� 2HCO3- Al��OH��3 + OH- �� AlO2- + 2H2O 3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O �Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3
CO32- + CO2 + H2O �� 2HCO3- Al��OH��3 + OH- �� AlO2- + 2H2O 3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O �Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3 ![]()
����������1����A��B��C��Ϊ����ͬ�ַǽ���Ԫ�صĻ����AΪʹʪ��ĺ�ɫʯ����ֽ���������壬A�ⰱ����B�Ӵ��������̱�ΪC��BΪNO��CΪNO2����Ӧ���Ļ�ѧ����ʽΪ![]() ����2����A��B��CΪ��ɫ��Ӧ���ʻ�ɫ�Ļ����A��B��C�ֱ�ΪNa2O2 ��Na2O ��Na2CO3��NaHCO3��XΪ��ɫ��ζ���壬XΪCO2����Ӧ�������ӷ���ʽΪCO32- + CO2 + H2O �� 2HCO3- ����3����A��B��C��Ϊ����ͬ�ֽ���Ԫ�صĻ����A��B��C�ֱ�Ϊ���Ρ�������������ƫ�����Σ�X��ǿ���Ӧ�������ӷ���ʽΪAl��OH��3 + OH- �� AlO2- + 2H2O����4����AΪ����Fe��XΪϡ���ᣬ��BΪ�����Σ�CΪ���Σ���Ӧ�������ӷ���ʽΪ3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O������B����Һ�м�������������Һ������Fe��OH��2�����ڿ���������������Ϊ�Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����Ӧ�Ļ�ѧ����ʽΪ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3 ����5����A��X��Ϊ���ʣ�BΪ��ʹƷ����Һ��ɫ�����壬B�Ƕ�������A����C������������Ӧ���Ļ�ѧ����ʽΪ
����2����A��B��CΪ��ɫ��Ӧ���ʻ�ɫ�Ļ����A��B��C�ֱ�ΪNa2O2 ��Na2O ��Na2CO3��NaHCO3��XΪ��ɫ��ζ���壬XΪCO2����Ӧ�������ӷ���ʽΪCO32- + CO2 + H2O �� 2HCO3- ����3����A��B��C��Ϊ����ͬ�ֽ���Ԫ�صĻ����A��B��C�ֱ�Ϊ���Ρ�������������ƫ�����Σ�X��ǿ���Ӧ�������ӷ���ʽΪAl��OH��3 + OH- �� AlO2- + 2H2O����4����AΪ����Fe��XΪϡ���ᣬ��BΪ�����Σ�CΪ���Σ���Ӧ�������ӷ���ʽΪ3Fe2+ + NO3- + 4H+ �� 3Fe3+ + NO + 2H2O������B����Һ�м�������������Һ������Fe��OH��2�����ڿ���������������Ϊ�Ȳ�����ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����Ӧ�Ļ�ѧ����ʽΪ Fe��OH��2 + O2 + 2H2O �� 4Fe��OH��3 ����5����A��X��Ϊ���ʣ�BΪ��ʹƷ����Һ��ɫ�����壬B�Ƕ�������A����C������������Ӧ���Ļ�ѧ����ʽΪ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������ԭ��Ӧ��2Cu(IO3)2+24KI+12H2SO4=2CuI��+13I2+12K2SO4+12H2O������1mol�������ڷ�Ӧ�еõ��ĵ���Ϊ��������
A. 10mol B. 11mol C. 12mol D. 13mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����Բ��ϣ�ͨʽΪMO��xFe2O3��MΪ���۽������ӣ�����Fe3O4�ɱ�ʾΪFeO��Fe2O3���Ʊ�����Ϊ��
![]()
��������ش�
��1���ֳ�ȡ2.8 g���ۣ�����һ������ϡ����ʹ����ȫ�ܽ���ټ���_____g��FeCl3���壬��������Ӧ���ɵõ�������Fe3O4��
��2�������MgSO4��FeCl3Ϊԭ�ϣ�Ҫ���18.0��MgO��2Fe2O3������ȡ������������Ҫ1 mol/L��NaOH��Һ____mL��
��3����һ���Ʊ�Fe3O4��ʵ���У����ڷ�Ӧ��������Ʋ������������һ�ֲ�Ʒ��ȡһ�����ò�Ʒ�������������У�����ͨ���״����672 mLCl2���ܰ���Һ�е�Fe2+ȫ������ΪFe3+��Ȼ���������Һ���ɣ����������أ���9.6 g���塣�ò�Ʒ�Ļ�ѧʽΪ_______��
��4����һ���ڵ��ӹ�ҵ��Ӧ�ù㷺�ĺ��������壬����ɿɱ�ʾΪ��![]() ������15.2 g FeSO4����Cr2O72-��H2O2�����ʴ����������뺬�����ʣ����ɵõ������������������ΧΪ___________________��
������15.2 g FeSO4����Cr2O72-��H2O2�����ʴ����������뺬�����ʣ����ɵõ������������������ΧΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ȷ����
A.����ʱ��Ϊ�˼ӿ�������ʣ����ò������ڹ������ڽ���
B.��������������Һʱ�����ȱ��ò��������裬ֱ��Һ��ȫ������
C.��ȡ����ʱ��Ӧѡ���л���ȡ��������ȡ�����ܶȱ����ˮ��
D.��Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��д�����Ba2+��OH����NO3������Һ�У������ܴ�������������ǣ�������
A.H+
B.NH4+
C.CO32��
D.Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ݸ�Ŀ���������վƵ����칤�գ������ỵ֮�ƣ��Կ��������������վƸ��ն���������ֵ����Ҳ���������õ���ʵ�鷽�������ڷ���
A.����ˮB.�Ҵ���ˮC.ʳ��ˮ����ɳD.����غ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A.ʯ����ֽ��pH��ֽʹ��ǰ������������ˮ��ʪ
B.�����ܽ�ﵽƽ��ʱ����Һ�����ʵ�����Ũ����ȣ��ұ��ֲ���
C.�����ˮ�ⷴӦ�������ȹ���
D.��ʽ�ε�pH��С��7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����У���Ҫ�ӿ컯ѧ��Ӧ���ʵ��ǣ�������
A.����
B.������ʴ
C.ʳ�︯��
D.�����ϻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ����
A. ֱ������1 nm��100 nm֮������ӳ�Ϊ����
B. �������ķ������Խ��������Һ����
C. ˮ�೧���ø�ѹ�����������Ϊ�����Ӵ����
D. ���ȼ����壬�ܷ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com