
钛被称为21世纪金属,是研制卫星、火箭、宇宙飞船及深海潜艇的重要材料。研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用下图所示装置模拟获得金属钙(需定期更换石墨棒),并以钙为还原剂,还原二氧化钛制备金属钛。下列叙述正确的是( )
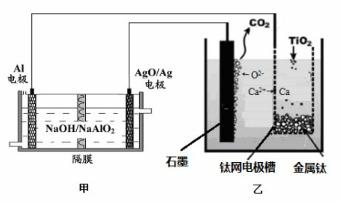
A. 甲装置工作过程中OH-向AgO/Ag极移动;乙装置工作过程中O2-向阴极移动
B. 若电解金属钛效率为![]() ,则获取1mol Ti时消耗Al的物质的量为
,则获取1mol Ti时消耗Al的物质的量为![]()
C. 乙装置阳极的电极反应式为![]()
D. 在制备金属钛前后,整套装置中CaO的总量减少
科目:高中化学 来源: 题型:阅读理解
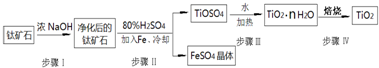
| 高温 |
| 高温 |
查看答案和解析>>
科目:高中化学 来源:2012届浙江省苍南县灵溪二高高三第二次月考化学试卷(带解析) 题型:单选题
被称为“21世纪金属”的钛金属(Ti)有多种同位素,如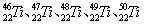 等。这些同位素原子的中子数不可能为
等。这些同位素原子的中子数不可能为
| A.30 | B.28 | C.26 | D.24 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省苍南县灵溪二高高三第二次月考化学试卷(解析版) 题型:选择题
被称为“21世纪金属”的钛金属(Ti)有多种同位素,如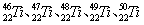 等。这些同位素原子的中子数不可能为
等。这些同位素原子的中子数不可能为
A.30 B.28 C.26 D.24
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

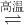 TiCl4(g)+O2(g);△H=+151kJ/mol
TiCl4(g)+O2(g);△H=+151kJ/mol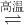 2MgCl2+Ti
2MgCl2+Ti查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com