
下列关于晶体的说法一定正确的是( )
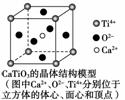
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻
C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
科目:高中化学 来源: 题型:
用溶质质量分数为98%的浓硫酸和溶质质量分数为18%的稀硫酸配制500 g溶质质量分数为28%的硫酸,需要浓硫酸和稀硫酸的质量分别为( )
A.62.5 g 437.5 g B.71.4 g 428.6 g
C.437.5 g 62.5 g D.428.6 g 71.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是( )
A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子
B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子
C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高
D.如果某一基态3p能级上仅有2个电子,它们自旋方向必然相反
查看答案和解析>>
科目:高中化学 来源: 题型:
H2O与H2S结构相似,都是V形的极性分子,但是H2O的沸点是100℃,H2S的沸点是-60.7℃。引起这种差异的主要原因是( )
A.范德华力 B.共价键
C.氢键 D.相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于晶体的说法中,正确的是( )
A.在晶体中只要有阴离子就一定有阳离子 B.在晶体中只要有阳离子就一定有阴离子
C.原子晶体的熔点一定比金属晶体的高 D.分子晶体的熔点一定比金属晶体的低
查看答案和解析>>
科目:高中化学 来源: 题型:
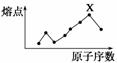
原子序数小于18的八种连号元素,它们的单质熔点随原子序数增大而变化的趋势如图所示,图中X元素应属于( )
A.ⅢA族 B.ⅣA族
C.ⅤA族 D.ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2∶1。请回答下列问题:
(1)A单质、B单质、化合物R的熔点大小顺序为下列的________(填序号)。
①A单质>B单质>R ②R>A单质>B单质
③B单质>R>A单质 ④A单质>R>B单质
(2)在CB3分子中C元素原子的原子轨道发生的是______杂化,其固体时的晶体类型为________。
(3)写出D原子的核外电子排布式:______________________________。C的氢化物比D的氢化物在水中的溶解度大得多的可能原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下每个选项中的两组物质都能反应,且能放出同一种气体的是( )
A.铜与稀硫酸,铜与浓硫酸
B.铁与稀硫酸,铁与浓硫酸
C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸
D.硫化钠与稀硫酸,硫化钠与稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素X,其原子的电子层数为(n-1),最外层电子数为(2n-1)。下列有关元素X的说法中正确的是( )
A.X可能是金属元素
B.由X形成的含氧酸均为强酸
C.X不能形成化学式为KXO4的含氧酸盐
D.元素X的气态氢化物一定极易溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com