
| A. | 25℃时,1LpH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA | |
| B. | 室温下,14.0g乙烯和丁烯的混合气体中含有的C-H键数目为2NA | |
| C. | 0.1molFe在0.1molCl2中充分燃烧,转移的电子数为0.3NA | |
| D. | 标准状况下,22.4LCCl4中含有的分子数目为NA |
分析 A、pH=12的Ba(OH)2溶液中c(OH-)=0.01mol/L;
B、乙烯和丁烯的最简式均为CH2;
C、0.1mol铁和0.1mol氯气反应,氯气不足;
D、标况下四氯化碳为液态.
解答 解:A、pH=12的Ba(OH)2溶液中c(OH-)=0.01mol/L,故1L溶液中氢氧根的物质的量为n=CV=0.01mol/L×1L=0.01mol,个数为0.01NA个,故A错误;
B、乙烯和丁烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为n=$\frac{14g}{14g/mol}$=1mol,故含2molC-H键,个数为2NA个,故B正确;
C、0.1mol铁和0.1mol氯气反应,氯气不足,由于氯气反应后变为-1价,故0.1mol氯气转移0.2mol电子即0.2NA个,故C错误;
D、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和分子数目,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Co2O3 | B. | Co3O3 | C. | Co3O4 | D. | Co5O7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
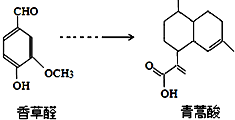
| A. | 青蒿酸分子中含有4个手性碳原子 | |
| B. | 在一定条件,香草醛可与HCHO发生缩聚反应 | |
| C. | 两种物质分别和H2反应,最多消耗H24mol和3mol | |
| D. | 可用FeCl3溶液或NaHCO3溶液鉴别化合物香草醛和青蒿酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若T1=T2,则x1>x2 | B. | 若T1=T2,则x1<x2 | C. | 若T1<T2,则x1=x2 | D. | 若T1<T2,则x1<x2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
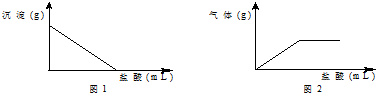 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )| A. | 取样溶于水,有白色沉淀产生,说明原白色固体中一定有Na2SO4和BaCl2 | |
| B. | 取样溶于水,静置后测得上层清液的pH>7,说明原白色固体中一定有NaOH | |
| C. | 取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,沉淀的量与加入盐酸体积的关系如图1所示,则原白色固体中无Na2SO4 | |
| D. | 取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,产生气体的量与加入盐酸体积的关系如图2所示,则该白色固体中无NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
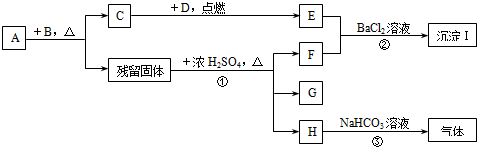
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com