
分析 (1)O元素的化合价降低,体现氧化性;
(2)O元素的化合价既升高又降低;
(3)根据还原剂生成的产物为氧化产物判断;
(4)根据氧化剂氧化性大于氧化产物的氧化性判断.
解答 解:A.Na2O2+2HCl═2NaCl+H2O2,该反应中各元素的化合价没有变化,所以不是氧化还原反应;
B.Ag2O+H2O2═2Ag+O2+H2O,根据化合价的变化知,氧化剂是Ag2O,还原剂是H2O2,Ag2O的氧化性大于H2O2的氧化性,O2为氧化产物;
C.2H2O2═2H2O+O2,根据化合价的变化知,H2O2既是氧化剂又是还原剂;
D.3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O,根据化合价的变化知,H2O2是氧化剂,K2CrO4是氧化产物,
(1)以上反应中H2O2仅体现氧化性的反应为D,
故答案为:D;
(2)以上反应中H2O2既体现氧化性又体现还原性的反应是C,
故答案为:C;
(3)以上反应中,B反应Ag2O+H2O2═2Ag+O2+H2O,根据化合价的变化知,氧化剂是Ag2O,还原剂是H2O2,生成的O2为氧化产物,
故答案为:O2;
(4)反应Ag2O+H2O2═2Ag+O2↑+H2O中,氧化银做氧化剂,双氧水作还原剂,则氧化性Ag2O>H2O2,
反应3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O中,双氧水做氧化剂,铬酸钾做氧化产物,则氧化性H2O2>K2CrO4,
故答案为:Ag2O>H2O2>K2CrO4.
点评 本题考查氧化还原反应,为高考常见题型,侧重氧化还原反应基本概念的考查,把握反应前后元素化合价的变化判断其氧化性、还原性即可,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 锌片发生氧化反应 | B. | 电子由锌片通过导线流向铜片 | ||
| C. | 铜片反应式为Cu2++2e-═Cu | D. | 该电池的反应本质是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
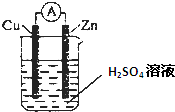 某学习小组针对化学能转变为其他形式的能量,进行如下实验:
某学习小组针对化学能转变为其他形式的能量,进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
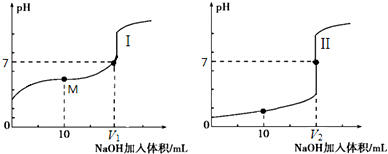
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
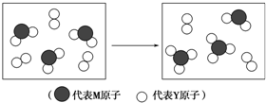
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Ⅰ | A、B、C、D、E、F、G七种短周期元素的原子序数依次增大 |
| Ⅱ | A和E同主族,B和F同主族,D和G同主族 |
| Ⅲ | A原子核内只有质子没有中子,B原子最外层电子数是电子层数的2倍 |
| Ⅳ | D和F以原子个数比为2:1组成的物质X是光导纤维的主要成分 |
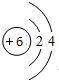 ,物质X的化学式为SiO2
,物质X的化学式为SiO2查看答案和解析>>
科目:高中化学 来源: 题型:解答题

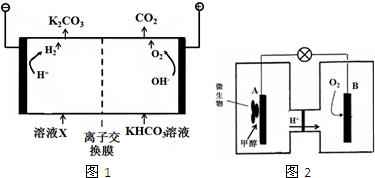
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4 L氢气含有的氢分子数为NA | |
| B. | 常温常压下,18 g水含有的原子数为3NA | |
| C. | 23g Na在氧气中完全燃烧转移的电子数为 2NA | |
| D. | 0.3 mol/LNa2SO4溶液中含有Na+的数目为0.6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com