
��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��
��1��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK=
��2�������¶ȣ��÷�ӦKֵ ����������ת���� ����ѧ��Ӧ���� �����Ͼ�������С�䣩��
��3��600��ʱ����һ�ܱ������У������������������ϣ���Ӧ������SO2��O2��SO3���ʵ����仯��ͼ����Ӧ����ƽ��״̬��ʱ���� ��

��4����ͼ�жϣ���Ӧ������20minʱ�����߷����仯��ԭ���� �������ֱ����
��5��10min��15min�����߱仯��ԭ������� ����д��ţ���
a�����˴��� b����С�������
c�������¶� d������SO3�����ʵ�����
��6����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬���ǣ� ��
a�� v��SO3����2v��O2�� b��������ѹǿ���ֲ���
c��v�棨SO2��=2v����O2�� d���������������ʵ��ܶȱ��ֲ���
��7��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ����ǣ� ��
a����ʱ�����SO3���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч�Ĵ���
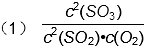
��2����������С
��3��15-20min��25-30min
��4��������������Ũ�Ȼ�����0.04mol����
��5��ab��6��bc��7��c
��������
��2���÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ�����ƶ���ƽ�ⳣ��k����������ת�����������¶ȷ�Ӧ���ʼ�С��
�ʴ�Ϊ����������С��
��3����Ӧ���������ʵ����ʵ������仯��˵����Ӧ����ƽ��״̬����ͼ��֪��15-20min��25-30min����ƽ̨������ֵ����ʵ������䣬��Ӧ����ƽ��״̬��
�ʴ�Ϊ��15-20min��25-30min��
��4����ͼ��֪����Ӧ������20minʱ��ƽ��������Ӧ�ƶ���˲��ֻ��������Ũ������Ӧ��������������Ũ�ȡ��ʴ�Ϊ��������������Ũ�ȡ�
��5����ͼ��֪����Ӧ������Ӧ���У�10min��15min��Ӧ����ﵥλʱ���ڵı仯������˵����Ӧ��������10min�ı�˲�䣬�����ʵ����ʵ������䡣
a�����˴���������Ӧ���ʣ���a��ȷ��
b����С�������������ѹǿ������Ӧ���ʣ���b��ȷ��
c�������¶ȷ�Ӧ���ʽ��ͣ���c����
d��10min�ı�˲�䣬�����ʵ����ʵ������䣬��������SO3�����ʵ�������d����
��ѡ��ab
��6��bc��7��c
���㣺����ƽ�ⳣ����ƽ���ƶ���ƽ��Ӱ��Ԫ�ء���ѧƽ��ͼ��ȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���л�ѧ������ȷ���ǣ� ��
A���۱�ϩ�Ľṹ��ʽ��
B�����Ȼ�̼���ӵĵ���ʽ��
C��2-�һ�-1,3-����ϩ���ӵļ���ʽ��
D��������ӵı���ģ�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�����ܱ������У����淴ӦA(s) B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
B + C(g) ��Q���ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
A������B��״ֻ̬��Ϊ��̬��Һ̬
B��ƽ��ʱ����λʱ����n(A)�����sn(C)����=1�s1
C������������䣬��ƽ����ϵ�м���B��ƽ��������淴Ӧ�����ƶ�
D������ʼʱ�������м���1molB��1molC���ﵽƽ��ʱ�ų�����Q
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и߶���ѧ����ĩ������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ʾ���ʱ仯�ķ�Ӧʽ�У���������
A��������ʴʱ���ܷ�����������Ӧ��2H2O + O2 + 4e�� = 4OH��
B����KHSO4��Һ�е���Ba(OH)2��ҺʹpH=7��SO42�� + 2 H+ + Ba2+ + 2OH��= BaSO4��+ 2 H2O
C������ˮ������ӷ���ʽ��Al3+ + 3H2O Al(OH)3 + 3H+
Al(OH)3 + 3H+
D��K37ClO3��Ũ����(HCl)�ڼ���ʱ����������K37ClO3 + 6HCl�� K37Cl + 3Cl2��+ 3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и߶���ѧ����ĩ������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶������£������Ѵﵽƽ��ķ�Ӧ��
FeCl3 +3KSCN  3KCl+Fe��SCN��3 ���ڴ���Һ�������´�����ƽ�����Ƶ���
3KCl+Fe��SCN��3 ���ڴ���Һ�������´�����ƽ�����Ƶ���
A�����������Ȼ��ع��� B�����������Ȼ�������
C������Fe��SCN��3��Ũ�� D����ˮϡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£��ܱ�������X��Y��Z��W��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±�������˵���������
���� | X | Y | Z | W |
��ʼŨ��/mol��L-1 | 0.5 | 0.6 | 0 | 0 |
ƽ��Ũ��/mol��L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
A����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ80%
B���÷�Ӧ��ƽ�ⳣ������ʽΪK=
C������ѹǿ��ƽ�ⳣ�����䣬��ʹƽ��������Z�ķ����ƶ�
D���ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ʾ���ʱ仯�ķ�Ӧʽ�У���������
A��������ʴʱ���ܷ�����������Ӧ��2H2O + O2 + 4e�� = 4OH��
B����KHSO4��Һ�е���Ba(OH)2��ҺʹpH=7��SO42�� + 2 H+ + Ba2+ + 2OH��= BaSO4��+ 2 H2O
C������ˮ������ӷ���ʽ��Al3+ + 3H2O Al(OH)3 + 3H+
Al(OH)3 + 3H+
D��K37ClO3��Ũ����(HCl)�ڼ���ʱ����������K37ClO3 + 6HCl�� K37Cl + 3Cl2��+ 3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����в������и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����dz�����ǿ���������㷺����ˮ����ϵͳ����ȡ�����ķ����ܶ࣬���и�ѹ�ŵ編�͵�ⴿˮ��ԭ������ͼ��ʾ�������й�˵������ȷ����


A����ѹ�ŵ編����Ӧ��ԭ��Ϊ3O2 2O3
2O3
B����ѹ�ŵ�����Ŀ����У�������������е���������
C�����ʱ���缫b��Χ�����ĵ缫��Ӧ��3H2O��6e����O3����6H����2H2O��4e����O2����4H��
D�����ʱ��H���ɵ缫a���ۺϹ�������Ĥ����缫b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ��У�߶���ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ������
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1�����÷�Ӧ��6NO2��8NH3 7N2��12H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״���µ������ L��
7N2��12H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״���µ������ L��
��2������֪��2SO2(g)+O2(g) 2SO3(g) ��H��?196.6 kJ��mol�C1
2SO3(g) ��H��?196.6 kJ��mol�C1
2NO(g)+O2(g) 2NO2(g) ��H��?113.0 kJ��mol�C1
2NO2(g) ��H��?113.0 kJ��mol�C1
��д��NO2��SO2��Ӧ����SO3(g)��NO���Ȼ�ѧ����ʽ ��
��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��� d��ÿ����1 mol SO2��ͬʱ����1 molNO2
�����������Ӧƽ��ʱNO2��SO2�����Ϊ1:6����÷�Ӧ��ƽ�ⳣ��K�� ��
��3������β���е�һ����̼��ͨ�����·�Ӧ������Ũ�ȣ�CO(g)+1/2O2(g) CO2(g)����֪ij�¶����������������ܱ������н�������Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±���ʾ�����á���������������д���еĿո�
CO2(g)����֪ij�¶����������������ܱ������н�������Ӧ�������и����ʵ���ʼŨ�ȼ������淴Ӧ���ʹ�ϵ���±���ʾ�����á���������������д���еĿո�
������� | c(CO)��mol��L�C1 | c(O2)��mol��L�C1 | c(CO2)��mol��L�C1 | ��(��)����(��) ��С�Ƚ� |
�� | 2.0��10�C4 | 4.0��10�C4 | 4.0��10�C4 | ��(��)����(��) |
�� | 1.0��10�C3 | 4.0��10�C4 | 5.0��10�C4 | ��(��) ��(��) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com