
| A. | IO-中碘元素的化合价为+l价 | |
| B. | 以上两反应均为氧化还原反应 | |
| C. | 以上两反应均为离子反应 | |
| D. | 反应②中,消耗1molH2O2,生成22.4LO2 |
科目:高中化学 来源: 题型:选择题

| A. | 甲能使酸性KMnO4溶液褪色 | |
| B. | 乙可与溴水发生取代反应而使溴水褪色 | |
| C. | 丙与浓硫酸、浓硝酸的混合液共热发生取代反应 | |
| D. | 丁不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解食盐水制得金属钠 | |
| B. | 电解熔融的氧化铝制取金属铝,用铁作阳极 | |
| C. | 一氧化碳高温还原铁矿石制得铁 | |
| D. | 电解法精炼粗铜,用纯铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol水和1mol水的摩尔质量 | |
| B. | 1 mol•L-1CaCl2溶液与2 mol•L-1KCl溶液中Cl-的物质的量 | |
| C. | 50Ml.1 mol•L-1MgCl2溶液与100Ml.1mol•L-1NaCl溶液中Cl-物质的量浓度 | |
| D. | 20%NaOH溶液与10%NaOH溶液中NaOH的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
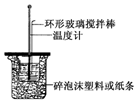 如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是减少热量损失;反应需要测量温度,每次测量温度后都必须采取的操作是用水将温度计冲洗干净并用滤纸擦干.
如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是减少热量损失;反应需要测量温度,每次测量温度后都必须采取的操作是用水将温度计冲洗干净并用滤纸擦干.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n(NaCl):n(NaClO):n(NaClO3)可能为8:3:l | |
| B. | 当通入氯气的物质的量为1mol时,生成NaClO3越多,则转移电子数越多 | |
| C. | 氯气与氢氧化钠反应,还原产物一定为NaCl | |
| D. | 若通入标况下氯气89.6L,且生成NaClO、NaClO3混合体系比值为1:1,则转移电了物质的量为4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 向某一溶液中滴加Ba(NO3)2和HNO3混合溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 向盛有2mL0.1mol/LAgNO3溶液的试管中滴加1mL0.1mol/LNaCl溶液,再向其中滴加4~5滴0.1mol/LKI溶液 | 先有白色沉淀成,后又产生黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| C | 室温下,取相同大小、形状和质量的Cu粒分别投入0.1mol/L的稀硝酸和10.0mol/L的浓硝酸中 | Cu粒与浓硝酸反应比与稀硝酸反应剧烈 | 探究浓度对化学反应速率的影响 |
| D | 向某一溶液中滴加稀盐酸,将生成的气体通入澄清石灰水中 | 澄清石灰水变浑浊 | 生成的气体可能是SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com