
某温度下,已知醋酸的电离常数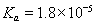 ,醋酸银的溶度积
,醋酸银的溶度积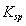 (CH3COOAg )=1.6×10
(CH3COOAg )=1.6×10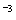 ,
,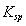 (Ag2CO3)=8.3
(Ag2CO3)=8.3 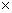 l0
l0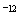 。在不考虑盐类水解的情况下,下列有关说法正确的是
。在不考虑盐类水解的情况下,下列有关说法正确的是
A.醋酸水溶液中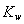 不变,故醋酸对水的电离无影响
不变,故醋酸对水的电离无影响
B.该温度下饱和醋酸水溶液的pH =5-lgl.8
C.该温度下浓度均为0.01 mol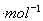 的CH3COONa溶液和AgNO3,溶液等体积混合(混合溶液体积具有加和性),有CH3COOAg沉淀生成
的CH3COONa溶液和AgNO3,溶液等体积混合(混合溶液体积具有加和性),有CH3COOAg沉淀生成
D.将0.02 mol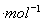 的Na2CO3,溶液与CH3COOAg沉淀上清液等体积混合,出现白色沉淀
的Na2CO3,溶液与CH3COOAg沉淀上清液等体积混合,出现白色沉淀
D
【解析】
试题分析:A水是弱电解质,存在电离平衡H2O H++OH-。当向水中加入CH3COOH时,醋酸电离产生的H+使溶液中的H+浓度增大,对水的电离平衡起到了抑制作用。错误。B.PH为溶液中c(H+)的负对数。
H++OH-。当向水中加入CH3COOH时,醋酸电离产生的H+使溶液中的H+浓度增大,对水的电离平衡起到了抑制作用。错误。B.PH为溶液中c(H+)的负对数。 .
.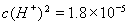 ;
;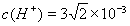 .所以pH=3- lg
.所以pH=3- lg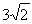 。错误。C.若二者等体积混合,则c(CH3COO-)·c(Ag+)= 0.005mol/L×0.005mol/L= 2.5×10-5 mol2/L2 <1.6×10-3=醋酸银的溶度积Ksp (CH3COOAg ).因此不会有CH3COOAg沉淀生成。错误。D.若将0.02 mol/L的Na2CO3溶液与CH3COOAg沉淀上清液等体积混合,c(CO32-)=0.01mol/L; c(Ag+)= 1/2×4 ×10-2 mol/L=2×10-2mol/L. c(CO32-)·c(Ag+)2=0.01mol/L×(2×10-2mol/L)2=4×10-6mol3/L3>8.3 ×l0-12.因此会出现Ag2CO3白色沉淀。正确。
。错误。C.若二者等体积混合,则c(CH3COO-)·c(Ag+)= 0.005mol/L×0.005mol/L= 2.5×10-5 mol2/L2 <1.6×10-3=醋酸银的溶度积Ksp (CH3COOAg ).因此不会有CH3COOAg沉淀生成。错误。D.若将0.02 mol/L的Na2CO3溶液与CH3COOAg沉淀上清液等体积混合,c(CO32-)=0.01mol/L; c(Ag+)= 1/2×4 ×10-2 mol/L=2×10-2mol/L. c(CO32-)·c(Ag+)2=0.01mol/L×(2×10-2mol/L)2=4×10-6mol3/L3>8.3 ×l0-12.因此会出现Ag2CO3白色沉淀。正确。
考点:考查电离平衡、水解平衡、沉淀溶解平衡的知识。


科目:高中化学 来源: 题型:

| c2(C) |
| c(A)×c3(B) |
| c2(C) |
| c(A)×c3(B) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 下列物质 ①Cu ②液态SO2 ③纯醋酸 ④NaHCO3 ⑤Ba(OH)2溶液
下列物质 ①Cu ②液态SO2 ③纯醋酸 ④NaHCO3 ⑤Ba(OH)2溶液查看答案和解析>>
科目:高中化学 来源:山东省兖州市2010-2011学年高二上学期期末考试化学试题 题型:022
下列
物质①Cu
②液态SO2
③纯醋酸
④NaHCO3
⑤Ba(OH)2溶液
Ⅰ、属于非电解质的是________;(填序号)
Ⅱ、(1)NaHCO3是一种________(填“强”或“弱”)电解质;
(2)写出HCO3―水解的离子方程式:________;
(3)常温下,0.1 mol·L-1 NaHCO3溶液的pH大于8,则溶液中Na+、HCO3―、H2CO3、CO32―、OH-五种微粒的浓度由大到小的顺序为:________.
(4)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1.若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1=________.(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=________.(已知:10-5.60=2.5×10-6)
Ⅲ、Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)该Ba(OH)2溶液的物质的量浓度为________;
(2)溶液中由水电离出c(OH―)=________;
(3)与某浓度盐酸溶液按体积比(碱与酸之比)1∶9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=________.
Ⅳ、醋酸是一种弱电解质.
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如下图所示.则图________(填“Ⅰ”或“Ⅱ”)为醋酸稀释的图像.
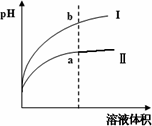
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山东省兖州市高二(上)期末化学试卷(解析版) 题型:解答题
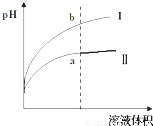
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com