
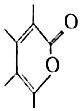
 以下说法正确的是( )
以下说法正确的是( )| A. | 一Me基团的电子式为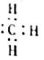 | |
| B. | 该合成过程的反应类型属于加成反应 | |
| C. | 产物与 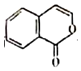 互为同分异构体 互为同分异构体 | |
| D. | 产物可与H2发生加成反应,反应的物质的量之比为1:3 |
分析 A.根据结构简式知,-Me表示甲基,甲基中碳原子上含有1个孤电子;
B.加成反应指有机物分子中的不饱和双键或叁键发生断裂,不饱和原子与其它原子或原子团直接结合生成新化合物的反应;
C. 的不饱和度是4,
的不饱和度是4, 的不饱和度是7,二者的分子式不同、结构不同;
的不饱和度是7,二者的分子式不同、结构不同;
D. 中只有碳碳双键能和氢气在一定条件下发生加成反应.
中只有碳碳双键能和氢气在一定条件下发生加成反应.
解答 解:A.根据结构简式知,-Me表示甲基,甲基中碳原子上含有1个孤电子,甲基的电子式为 ,故A错误;
,故A错误;
B.加成反应指有机物分子中的不饱和双键或叁键发生断裂,不饱和原子与其它原子或原子团直接结合生成新化合物的反应,根据加成反应概念知,该反应为加成反应,故B正确;
C. 的不饱和度是4,
的不饱和度是4, 的不饱和度是7,二者的分子式不同、结构不同,所以二者不是同分异构体,故C错误;
的不饱和度是7,二者的分子式不同、结构不同,所以二者不是同分异构体,故C错误;
D. 中只有碳碳双键能和氢气在一定条件下发生加成反应,所以产物可与H2发生加成反应,反应的物质的量之比为1:2,故D错误;
中只有碳碳双键能和氢气在一定条件下发生加成反应,所以产物可与H2发生加成反应,反应的物质的量之比为1:2,故D错误;
故选B.
点评 本题考查有机物结构和性质,为高频考点,侧重考查学生理解、分析、判断能力,明确基本概念、官能团及其性质关系是解本题关键,注意D中酯基不能发生加成反应,酯基和羧基中碳氧双键都不能发生加成反应,但醛基和羰基中碳氧双键能发生加成反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 常温下,4.2g乙烯和丙烯的混合气体中含有的非极性键总数为0.6NA | |
| B. | 电解精炼铜时,当电路中转移NA个电子,阳极溶解32 g铜 | |
| C. | 在含有CH3COO-为1.0 mol•L-1的醋酸溶液中,H+数目略大于NA | |
| D. | V L a mol•L-1的氯化铁溶液中,若Fe3+的数目为 NA,则Cl-的数目大于3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图I研究的是温度对反应的影响,且乙的温度较高 | |
| B. | 图Ⅱ研究的是压强对反应的影响,且甲的压强较高 | |
| C. | 图III研究的是温度对反应的影响,且乙的温度较低 | |
| D. | 图IV研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③⑤ | C. | ②④⑤⑥ | D. | ③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
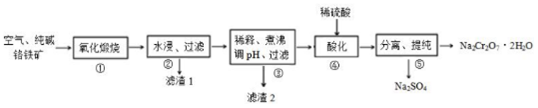
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
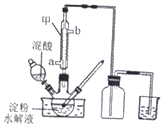 草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取、性质及应用,进行如下实验.
草酸(H2C2O4)是一种重要的有机化工原料.为探究草酸的制取、性质及应用,进行如下实验.| 编号 | H2C2O4溶液 | 酸性高锰酸钾溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-l | 体积/mL | ||
| 甲 | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| 乙 | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| 丙 | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com