
已知NA代表阿伏加德罗常数,下列说法正确的是
A.在1 L 0.1 mol·L-1氟化钠溶液中含有F-和HF数目之和为0.1NA
B.300 mL 2 mol/L蔗糖溶液中所含分子数为0.6NA
C.标准状况下,1.8gD2O中含有NA个中子
D.标准状况下,2.24 L三氯甲烷中含有氯原子数目为0.3NA
科目:高中化学 来源:2016届河南省高三第二次月考化学试卷(解析版) 题型:选择题
下列各组离子能在指定环境中大量共存的是
A.在c(HCO3-)=0.1 mol·L-1的溶液中:NH4+、Al3+、Cl-、NO3-
B.在由水电离出的c(H+)=1×10-12mol·L-1的溶液中:Fe2+、ClO-、Na+、SO42-
C.在加入镁粉产生气体的溶液中:SO42-、NO3-、Na+、Fe2+
D.在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+
查看答案和解析>>
科目:高中化学 来源:2016届河北省冀州市高三复习班上第一次月考化学试卷A(解析版) 题型:选择题
下列制备和收集气体的实验装置合理的是

A.装置①:用氯化铵和氢氧化钙制NH3
B.装置②:用铜和稀硝酸制NO
C.装置③:用锌粒和稀硫酸制H2
D.装置④:用双氧水和二氧化锰制O2
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:选择题
从海水中制得的氯化钠除食用外,还可用作工业原料,生成多种含钠或氯的化工产品,利用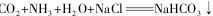 +NH4Cl的反应原理可制备纯碱,下面是在实验室进行模拟实验的生产流程示意图。
+NH4Cl的反应原理可制备纯碱,下面是在实验室进行模拟实验的生产流程示意图。
饱和食盐水溶液
则相关的说法错误的是
A.通入的气体:A是CO2,B是NH3
B.NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3和NH4Cl的溶解度都小
C.步骤(3)的操作为过滤,滤液可作化学肥料
D.步骤(4)中,将晶体加热分解可以得到纯碱
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第四次大考化学试卷(解析版) 题型:填空题
(14分)A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系。根据要求回答问题:
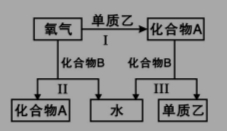
(1)上图三个反应中,属于氧化还原反应的有 个。
(2)若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有 。
A.还原性:H2R>H2O B.酸性:H2R>H2O
C.稳定性:H2R<H2O D.沸点:H2R<H2O
(3)若化合物B常温下为气体,其水溶液呈碱性(答题必须用具体物质表示)。
①化合物B的电子式为______;其水溶液呈碱性的原因是 (用离子方程式表示)。
反应III的化学方程式为______________________。
②化合物B可与O2组成燃料电池(氢氧化钾溶液为电解质溶液),其反应产物与反应Ⅲ相同。写出该电池负极的电极反应式______________________。
③当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为△H1和△H2,则反应Ⅰ的热化学方程式为______________(注:反应条件相同、所有物质均为气体)。
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:填空题
(共10分)A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大。A是宇宙中含量最高的元素,B可形成多种同素异形体,其中一种的硬度自然界中最大。D元素原子的最外层电子数是次外层电子数的3倍。E元素的最高价氧化物的水化物的酸性强于硫酸。
(1)写出元素C在元素周期表的位置 ,单质E的工业制备的离子方程式为________。
(2)B、C、D三种元素的最简单氢化物的稳定性从大到小的顺序是 (填化学式),
B的单质在加热条件下能与C的最高价氧化物对应的水化物的浓溶液反应,写出对应的化学方程式 。
(3)A、B、C、D几种元素之间可以形成多种10电子微粒,写出上述10电子微粒中离子之间反应的一个离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:选择题
下列有关实验的现象描述正确的是
A.氢气在氯气中燃烧,火焰呈苍白色,瓶口出现大量白雾
B.磷在氯气中燃烧,发出明亮的蓝紫色火焰,产生大 量白色烟雾
量白色烟雾
C.铜在氯气中燃烧,产生白烟,加水溶解后可得蓝绿色溶液
D.用洁净的铂丝沾取碳酸钾粉末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省五校协作体高三上学期期初考试化学试卷(解析版) 题型:实验题
(13分)Na2S2O3俗称大苏打(海波)是重要的化工原料。用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3。已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g。常温下,从溶液中析出的晶体是Na2S2O3·5H2O。
现实验室欲制取Na2S2O3·5H2O晶体(Na2S2O3·5H2O的分子量为248)步骤如下:
①称取12.6g Na2SO3于烧杯中,溶于80.0mL水。
②另取4.0g硫粉,用少许乙醇润湿后,加到上述溶液中。
③(如图所示,部分装置略去),水浴加热,微沸,反应约1小时后过滤。

④滤液在经过 、 后析出Na2S2O3·5H2O晶体。
⑤进行减压过滤并干燥。
(1)仪器B的名称是________。其作用是_____________。加入的硫粉用乙醇润湿的目的是 。
(2)步骤④应采取的操作是 、 。
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质是 。如果滤液中该杂质的含量不很低,其检测的方法是: 。
(4)为了测产品的纯度,称取7.40g 产品,配制成250mL溶液,用移液管移取25.00mL于锥形瓶中,滴加淀粉溶液作指示剂,再用浓度为0.0500mol/L 的碘水,用 (填“酸式”或“碱式”)滴定管来滴定(2S2O32- + I2 = S4O62- + 2I-),滴定结果如下:
滴定次数 | 滴定前读数(mL) | 滴定滴定后读数(mL) |
第一次 | 0.30 | 31.12 |
第二次 | 0.36 | 31.56 |
第三次 | 1.10 | 31.88 |
则所得产品的纯度为 ,你认为影响纯度的主要原因是(不考虑操作引起误差) 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一上学期第一次月考化学试卷(解析版) 题型:选择题
a g CO2中含有b个分子,则阿伏加德罗常数为
A.ab/44 mol-1 B.44b /a C.44b /a mol-1 D.22b /a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com