
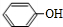
 +��CH3CO��2O��
+��CH3CO��2O��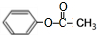 +CH3COOH��
+CH3COOH�� ��D�Ľṹ��ʽΪ
��D�Ľṹ��ʽΪ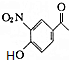 ��
��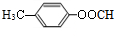 ����ṹ��ʽ��
����ṹ��ʽ��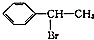 Ϊ��ʼԭ���Ʊ�
Ϊ��ʼԭ���Ʊ�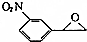 �ĺϳ�·�ߣ�
�ĺϳ�·�ߣ�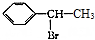 $��_{��}^{NaOHˮ��Һ}$
$��_{��}^{NaOHˮ��Һ}$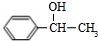 $��_{Cu/��}^{O_{2}}$
$��_{Cu/��}^{O_{2}}$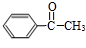 $��_{H_{3}PO_{4}}^{ŨHNO_{3}}$
$��_{H_{3}PO_{4}}^{ŨHNO_{3}}$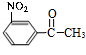 $\stackrel{NaBH_{4}}{��}$
$\stackrel{NaBH_{4}}{��}$ ��
�� ���� ��D�ķ���ʽ��E�Ľṹ��֪��D��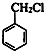 ����ȡ����Ӧ����E����DΪ
����ȡ����Ӧ����E����DΪ ��C����FeCl3��Һ������ɫ��Ӧ�����з��ǻ������C�ķ���ʽ���ƿ�֪CΪ
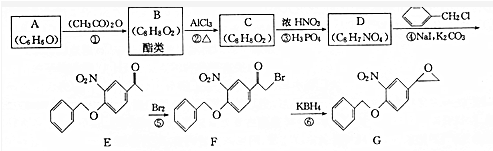
��C����FeCl3��Һ������ɫ��Ӧ�����з��ǻ������C�ķ���ʽ���ƿ�֪CΪ ��A�ķ���ʽΪC6H6O��A����������Ӧ�õ���B��B���Ȼ��������µõ�C����AΪ
��A�ķ���ʽΪC6H6O��A����������Ӧ�õ���B��B���Ȼ��������µõ�C����AΪ ��BΪ
��BΪ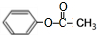 ��E���巢��ȡ����Ӧ����F���൱��E���ʻ���ԭΪ�ǻ����ٷ���ȡ����Ӧ�õ�F��
��E���巢��ȡ����Ӧ����F���൱��E���ʻ���ԭΪ�ǻ����ٷ���ȡ����Ӧ�õ�F��
��5�� ����������ˮ��Һ�����������·���ˮ�ⷴӦ����
����������ˮ��Һ�����������·���ˮ�ⷴӦ���� ����������������
���������������� ��������/���������·���ȡ����Ӧ����
��������/���������·���ȡ����Ӧ���� �������NaBH4�����·�Ӧ����
�������NaBH4�����·�Ӧ���� ��
��
��� �⣺��D�ķ���ʽ��E�Ľṹ��֪��D�� ����ȡ����Ӧ����E����DΪ
����ȡ����Ӧ����E����DΪ ��C����FeCl3��Һ������ɫ��Ӧ�����з��ǻ������C�ķ���ʽ���ƿ�֪CΪ
��C����FeCl3��Һ������ɫ��Ӧ�����з��ǻ������C�ķ���ʽ���ƿ�֪CΪ ��A�ķ���ʽΪC6H6O��A����������Ӧ�õ���B��B���Ȼ��������µõ�C����AΪ
��A�ķ���ʽΪC6H6O��A����������Ӧ�õ���B��B���Ȼ��������µõ�C����AΪ ��BΪ
��BΪ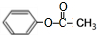 ��E���巢��ȡ����Ӧ����F���൱��E���ʻ���ԭΪ�ǻ����ٷ���ȡ����Ӧ�õ�F��
��E���巢��ȡ����Ӧ����F���൱��E���ʻ���ԭΪ�ǻ����ٷ���ȡ����Ӧ�õ�F��
��1��F�еĺ����������У��Ѽ����ʻ�����������Ӧ�ܵķ�Ӧ����Ϊȡ����Ӧ��
�ʴ�Ϊ���Ѽ����ʻ���������ȡ����Ӧ��
��2����Ӧ�ٵĻ�ѧ����ʽΪ�� +��CH3CO��2O��
+��CH3CO��2O��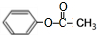 +CH3COOH��
+CH3COOH��
�ʴ�Ϊ�� +��CH3CO��2O��
+��CH3CO��2O��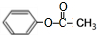 +CH3COOH��
+CH3COOH��
��3��C�Ľṹ��ʽΪ  ��D�Ľṹ��ʽΪ
��D�Ľṹ��ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��4��B��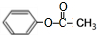 ����ͬ���칹�壨���������칹������ͬʱ��������������a���ܷ���������Ӧ��˵������ȩ����b������NaOH��Һ������Ӧ��˵��������������ǻ���c�����б����ṹ��
����ͬ���칹�壨���������칹������ͬʱ��������������a���ܷ���������Ӧ��˵������ȩ����b������NaOH��Һ������Ӧ��˵��������������ǻ���c�����б����ṹ��
��Ϊ�����γɵ�����������1��ȡ����������Ϊ���ᱽ����������2��ȡ����Ϊ-CH3��-OOCH�����ڡ��䡢��3�֣�
������ȩ�������ǻ�������2��ȡ����������һ��Ϊ-OH�������ȡ����Ϊ-CH2CHO�����ڡ��䡢��3�֣�����3��ȡ������Ϊ-OH��-CH3��-CHO����-OH��-CH3������λʱ��-CHO��4��λ�ã���-OH��-CH3���ڼ�λʱ��-CHO��4��λ�ã���-OH��-CH3���ڶ�λʱ��-CHO��2��λ�ã�
����������ͬ���칹�干��17�֣����к˴Ź���������ʾΪ4��壬�ҷ������Ϊ3��2��2��1����  ��
��
�ʴ�Ϊ��17�� ��
��
��5�� ����������ˮ��Һ�����������·���ˮ�ⷴӦ����
����������ˮ��Һ�����������·���ˮ�ⷴӦ���� ����������������
���������������� ��������/���������·���ȡ����Ӧ����
��������/���������·���ȡ����Ӧ���� �������NaBH4�����·�Ӧ����
�������NaBH4�����·�Ӧ���� ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ�� $��_{��}^{NaOHˮ��Һ}$
$��_{��}^{NaOHˮ��Һ}$ $��_{Cu/��}^{O_{2}}$
$��_{Cu/��}^{O_{2}}$ $��_{H_{3}PO_{4}}^{ŨHNO_{3}}$
$��_{H_{3}PO_{4}}^{ŨHNO_{3}}$ $\stackrel{NaBH_{4}}{��}$
$\stackrel{NaBH_{4}}{��}$ ��
��
�ʴ�Ϊ�� $��_{��}^{NaOHˮ��Һ}$
$��_{��}^{NaOHˮ��Һ}$ $��_{Cu/��}^{O_{2}}$
$��_{Cu/��}^{O_{2}}$ $��_{H_{3}PO_{4}}^{ŨHNO_{3}}$
$��_{H_{3}PO_{4}}^{ŨHNO_{3}}$ $\stackrel{NaBH_{4}}{��}$
$\stackrel{NaBH_{4}}{��}$ ��
��
���� ���⿼���л�����ƶ���ϳɣ��������ʵķ���ʽ��E�Ľṹ�����ƶϣ���5����ע�����ת������������Ϣ���кϳ�·����ƣ����ؿ���ѧ������������������ѧ������֪ʶǨ������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Ba2+��CO32-��NO3- | B�� | Na+��OH-��K+��MnO4- | ||
| C�� | K+��HCO3-��SO42-��Na+ | D�� | H+��Cl-��Cu2+��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
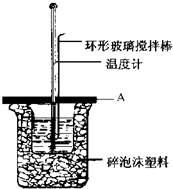 ��ͼ��ʾAΪ��ĭ���ϰ壬����������С�ף��ֱ�����¶ȼƺͻ��β��������������С�ײ��ܿ��ù�����Ŀ���Ǽ���������ʧ�� ��ʵ���в��Ӹ���ĭ���ϰ壬����õ��к�����ֵ����ƫ��ƫС����Ӱ�죩��
��ͼ��ʾAΪ��ĭ���ϰ壬����������С�ף��ֱ�����¶ȼƺͻ��β��������������С�ײ��ܿ��ù�����Ŀ���Ǽ���������ʧ�� ��ʵ���в��Ӹ���ĭ���ϰ壬����õ��к�����ֵ����ƫ��ƫС����Ӱ�죩���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �õ�صĸ���п������ԭ��Ӧ | |
| B�� | �õ�ط�Ӧ�ж���������������� | |
| C�� | ��0��lmol Zn��ȫ�ܽ�ʱ���������Һ�ĵ��Ӹ���ԼΪ1.204��1023 | |
| D�� | ���������ӦʽΪ MnO2+e-+H20�TMnO��OH��+OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
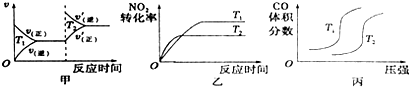
| Ũ��/mol��L-1/ʱ��/min | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl•�ڷ�Ӧ���Ǵ��� | |
| B�� | Cl•��Cl2������ | |
| C�� | ��Ҳ������Cl•��g��+CH4��g����CH3Cl��g��+H•��g�� | |
| D�� | �ɢۿ�֪C-Cl�ļ��ܱ�Cl-Cl�ļ���С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ��ʫ������ | ���еĻ�ѧ��Ӧ���� |
| A | �������г����꣬������ů������ | ���ֽⷴӦ |
| B | ǧ���������ɽ���һ���������� | �ֽⷴӦ |
| C | ���ϵ���˿����������ɻ���ʼ�� | ���Ϸ�Ӧ |
| D | ����»��»����ͭ | �û��ֽⷴӦ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2+��Na+��NO3-��Cl- | B�� | Ba2+��Cu2+��NO${\;}_{3}^{-}$��Cl- | ||
| C�� | SO42-��SO3-��NH4+��Na+ | D�� | Mg2+��Na+��Br-��ClO- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com