
【题目】某课外活动小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应为____________________。
(2)若开始时开关K与b连接,则B极的电极反应为____________________,总反应的离子方程式为____________________。
(3)有关上述实验,下列说法正确的是______。
A.溶液中Na+向A极移动
B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
D.若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
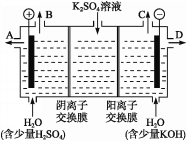
①该电解槽的阳极反应为______________。 此时通过阴离子交换膜的离子数_____(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填“A”、“B”、“C”或 “D”)________导出。
③电解过程中阴极区碱性明显增强,用平衡移动原理解释原因__________________________。
【答案】 Fe-2e- = Fe2+ 2H++2e- = H2↑ 2Cl-+2H2O![]() 2OH-+ H2↑+ Cl2↑ B 2H2O-4e- = 4H++ O2↑ 小于 D H2O
2OH-+ H2↑+ Cl2↑ B 2H2O-4e- = 4H++ O2↑ 小于 D H2O![]() H++ OH-,H+在阴极附近放电,引起水的电离平衡向右移动,使c(OH-)>c(H+)
H++ OH-,H+在阴极附近放电,引起水的电离平衡向右移动,使c(OH-)>c(H+)
【解析】试题分析:
(1) 开关K与a连接时,装置为原电池,铁为负极,发生吸氧腐蚀,即电极反应为Fe-2e-=Fe2+。
(2) 开关K与b连接时,装置为电解池,电解食盐水,此时阳极A发生2Cl--2e-=Cl2↑,阴极B发生2H++2e-H2↑,总反应的离子方程式为2Cl-+2H2O![]() 2OH-+ H2↑+ Cl2↑。
2OH-+ H2↑+ Cl2↑。
(3)阳离子向阴极移动,A错误;阳极A处产生的是Cl2,能使湿润的KI淀粉试纸变蓝,B正确;C应该通入HCl,不能加盐酸,因为盐酸是HCl的水溶液,错误;D电子不能在溶液中移动,错误。
(4))溶液中的OH-在阳极失电子产生O2:4OH--4e-=2H2O+O2↑,所以在B口放出O2,从A口导出H2SO4。溶液中的H+在阴极得到电子产生H2:2H++2e-=H2↑,则从C口放出H2,从D口导出KOH溶液。依据电荷守恒,通过阳离子交换膜的K+是通过阴离子交换膜的SO42-的2倍,所以通过阳离子交换膜的离子数大于通过阴离子交换膜的离子数。③电解过程中,H+在阴极附近放电,引起水的电离平衡向右移动,使c(OH-)>c(H+),故阴极区碱性明显增强。


科目:高中化学 来源: 题型:
【题目】(1)物质的量表示______的集合体。
(2)物质的量的符号______;单位______;阿伏加德罗常数的符号______;单位______;通常用______表示。
(3)摩尔质量的符号______;常用单位______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素B的核电荷数为Z,已知Bn﹣和Am+的核外具有相同的电子层结构,则A元素的原子序数用Z、n、m来表示,应为( )
A.Z+n﹣m
B.Z+m+n
C.Z﹣n﹣m
D.Z﹣n+m
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)-空气电池(如图)具有原料易得、能量密度高等优点,有望成为新能源汽车和移动设备的电源。该类电池在碱性环境下的总反应方程式为:4M+nO2+2nH2O=4M(OH)n。已知:电池的“理论比能量”指单位质量电极材料理论上释放出的最大电能。下列说法不正确的是( )
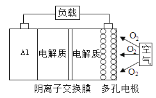
A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 比较Mg、Al、Zn三种金属-空气电池,Al-空气电池的理论比能量最高
C. M-空气电池放电过程的正极反应式:4Mn++nO2+2nH2O+4ne–=4M(OH)n
D. 消耗氧气22.4 L(标准状况),有4 molOH-从右往左通过阴离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯气的叙述中正确的是( )
A.若氯气发生泄漏,应立即向下风地区转移
B.氯气、氯水和液氯是同一种物质
C.氯气不能溶于水,所以可用排水法收集
D.用管子把氯气通入老鼠洞中可以灭鼠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,一定压强下的密闭容器中发生反应:aX(g)+bY(g) ![]() cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是
cZ(g)+dW(g),达平衡后,保持温度不变压强增大至原来的2倍,当再达到平衡时,W的浓度为原平衡状态的1.8倍,下列叙述正确是
A. 平衡正移 B. Z的体积分数变小
C. (a+b)>(c+d) D. X的转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述正确的是( )
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①过滤后所得沉淀为氢氧化铁
C. 电解法制取铝单质时也可以采用电解氯化铝以降低成本
D. 反应②的化学方程式为NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,与16g O2的体积相等的N2为( )
A.体积为22.4LB.分子数为6.02×1024
C.质量为14gD.物质的量为1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com