
【题目】近年来,由于石油价格不断上涨,以煤为原料制备一些化工产品的前景又被看好。如图是以煤为原料生产聚氯乙烯(PVC)和人造羊毛的合成路线。
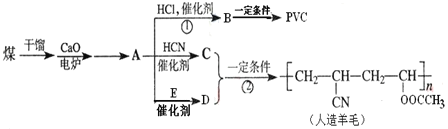
请回答下列问题:
(1)写出反应类型:反应①___;反应②___。
(2)写出结构简式:PVC___;E___。
(3)按要求写出化学方程式:
①→A:___;
②检验E中含氧官能团:___;
③Y+Z生成乙酸乙酯:___。
【答案】加成反应 加聚反应 ![]() CH3COOH
CH3COOH ![]() 加入碳酸氢钠溶液,有气泡产生 CH3COOH+CH3CH218OH
加入碳酸氢钠溶液,有气泡产生 CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O
CH3CO18OCH2CH3+H2O
【解析】
根据本题给出的信息,煤干馏得到焦炭,焦炭在电炉中和氧化钙发生反应,生成碳化钙,碳化钙与水反应生成炔,故A为乙炔,有官能团碳碳三键的性质;乙炔和氯化氢在催化剂的条件下发生加成反应,生成氯乙烯(B);在根据碳碳双键的性质,氯乙烯在一定的条件下发生加聚反应生成聚氯乙烯,既得PVC(![]() );乙炔和HCN发生加成反应生成(C)CH2═CHCN,根据将高分子化合物还原为单体的原理,将高分子化合物中的单键变双键,双键变单键,从双键不成立的地方断开原则,推出形成人造羊毛的单体为H2C═CH-OOCCH3和H2C═CH-CN,推出E是乙酸,A、E发生加成反应生成(D)H2C═CH-OOCCH3;CH2═CHCN和H2C═CH-OOCCH3都含有碳碳双键,故能发生加聚反应生成高分子化合物,人造羊毛。
);乙炔和HCN发生加成反应生成(C)CH2═CHCN,根据将高分子化合物还原为单体的原理,将高分子化合物中的单键变双键,双键变单键,从双键不成立的地方断开原则,推出形成人造羊毛的单体为H2C═CH-OOCCH3和H2C═CH-CN,推出E是乙酸,A、E发生加成反应生成(D)H2C═CH-OOCCH3;CH2═CHCN和H2C═CH-OOCCH3都含有碳碳双键,故能发生加聚反应生成高分子化合物,人造羊毛。
(1)反应①是乙炔和氯化氢发生加成反应;反应②是加聚反应生成聚合物;
(2)PVC的结构简式为: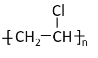 ;E是:CH3COOH;
;E是:CH3COOH;
(3)①→A的方程式为:![]() ;②检验E中含氧官能团羧基,加入碳酸氢钠溶液,有气泡产生;③乙酸与乙醇反应生成乙酸乙酯:CH3COOH+CH3CH2OH
;②检验E中含氧官能团羧基,加入碳酸氢钠溶液,有气泡产生;③乙酸与乙醇反应生成乙酸乙酯:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】关于![]() 的叙述错误的是( )
的叙述错误的是( )
A.是两性氢氧化物
B.是难溶于水的白色胶状物质,是弱电解质
C.既溶于氨水,又能溶于醋酸
D.能凝聚水中悬浮物,可用做净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是( )
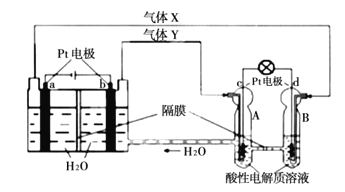
A. 当有0.8mol电子转移时,b极产生4.48LO2
B. 为了增加导电性可以将左边容器中的水改为NaOH溶液
C. d极上发生的电极反应是:2H+ +2e-=H2
D. c极上进行氧化反应,A池中的H+可以通过隔膜进入B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄血盐[亚铁氰化钾,K4Fe(CN)6]目前广泛用作食品添加剂(抗结剂),我国卫生部规定实验中黄血盐的最大使用量为10mg/kg。一种制备黄血盐的工艺如图:
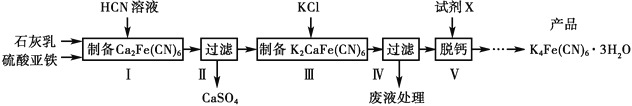
回答下列问题:
(1)步骤Ⅰ制备的Ca2Fe(CN)6易溶于水吗?__(填“易溶”或“不易溶”)。
(2)步骤Ⅲ的化学方程式为__。
(3)步骤Ⅴ所用的试剂X是__(填化学式)。
(4)工艺中用到剧毒的HCN溶液,含CN-的废水必须处理后才能排放。
已知:HCN是一种具有苦杏仁味的无色剧毒液体,易挥发,25℃时Ka(HCN)=6.25×10-10;溶液中H2CO3、HCO3-、CO32-的存在与溶液pH的关系如图所示:
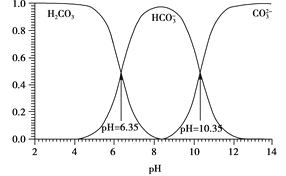
①HCN的电子式为__。
②处理含CN-废水的方法:第一步控制pH>10,用NaClO溶液先将CN-不完全氧化为OCN-;第二步控制pH为7.5~8.5,用NaClO溶液完全氧化OCN-生成N2和两种盐。第一步控制强碱性的主要目的是__,第二步反应的离子方程式为__。
(5)已知蓝色染料普鲁士蓝的合成方法如图:

用硫酸亚铁碱性试纸可以检验食品中是否含有CN-,方案如图:
![]()
若试纸变蓝则证明食品中含有CN-,基于普鲁士蓝的合成原理,请用离子方程式解释检测时试纸变蓝的原因:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示。已知①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;②有关有机物物的沸点如下表:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
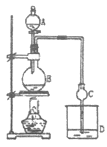
A中放醋酸,B中将过量的乙醇与少量浓硫酸混合,D中放有饱和碳酸钠溶液,经分液漏斗边滴加醋酸、边加热。
请回答:
(1)反应混合物的配制:圆底烧烧瓶中先加入___,再逐滴加入___,边加边振荡,___后,再加入醋酸。
(2)反应中加入的乙醇是过量的,其目的是___;浓硫酸的作用:①___;②___。
(3)该反应中,若用CH3CH218OH与乙酸发生反应,则反应的化学方程式为___。
(4)加热除了加快反应速率外还有一个重要的目的:___。
(5)在装置中,球形干燥管主要起到两个作用:一是起冷凝作用,二是:___。
(6)试管中盛放的是饱和碳酸钠溶液,它的作用是___(选填编号)。
A.中和乙酸和乙醇 B.吸收乙酸并溶解乙醇
C.降低乙酸乙酯的溶解度,有利于析出 D.加速乙酸乙酯的生成,提高其产率
(7)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出___;再加入___(此空从下列选项中选择),目的是___,然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.碱石灰 B.无水硫酸钠 C.生石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2,测得溶液中![]() 与
与![]() 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
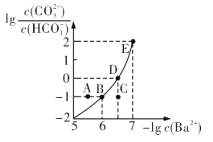
A.该溶液中![]()
B.B、D、E三点对应溶液pH的大小顺序为B>D>E
C.A、B、C三点对应的分散系中,A点的稳定性最差
D.D点对应的溶液中一定存在2c(Ba2+ ) +c(Na+ )+c(H+ )=c(CO32- )+c(OH- )+c(Cl- )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )
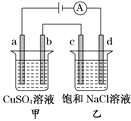
A. 电路中电子流向:负极→d→c→b→a→正极
B. a、c两极产生气体的物质的量相等
C. SO42-向b电极运动,Cl-向c电极运动
D. 通电后乙烧杯滴入酚酞溶液d极会变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将浓度均为0.5mol·L-1的氨水和KOH溶液分别滴入到两份均为20mLc1mol·L-1的AlCl3溶液中,测得溶液的导电率与加入碱的体积关系如图所示。下列说法正确的是
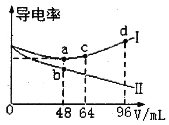
A.c1=0.2
B.b点时溶液的离子浓度:c(C1-)>c(NH4+)>c(OH-)>c(H+)
C.ac段发生的反应为:A1(OH)3+OH-==[Al(OH)4]-
D.d点时溶液中:c(K+)+c(H+)==[Al(OH)4]-+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个化学过程的示意图,请回答下列问题:
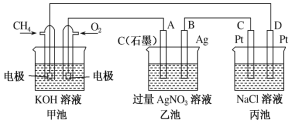
(1)图中甲池是____________装置,乙池是______________装置。
(2)D电极的名称是______________,A电极的名称是_______________。
(3)通入O2的电极的电极反应式为___________,通入CH4的电极的电极反应式为_________。
(4)丙池中反应的化学方程式为__________________。
(5)当乙池中B(Ag)极的质量增加4.32g时,甲池中理论上消耗O2______________________mL(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com