
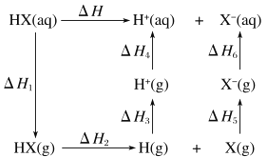
ЁОЬтФПЁПКьСзP(s)КЭCl2(g)ЗЂЩњЗДгІЩњГЩPCl3(g)КЭPCl5(g)ЁЃЗДгІЙ§ГЬКЭФмСПЙиЯЕШчЭМЫљЪО(ЭМжаЕФІЄHБэЪОЩњГЩ1molВњЮяЕФЪ§Он)ЁЃ

ИљОнЭМЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉPКЭCl2ЗДгІЩњГЩPCl3ЕФШШЛЏбЇЗНГЬЪНЪЧ__ЁЃ
ЃЈ2ЃЉPCl5ЗжНтГЩPCl3КЭCl2ЕФШШЛЏбЇЗНГЬЪНЪЧ__ЁЃ
ЃЈ3ЃЉPКЭCl2ЗжСНВНЗДгІЩњГЩ1molPCl5ЕФІЄH3=_ЃЌPКЭCl2вЛВНЗДгІЩњГЩ1molPCl5ЕФІЄH4__ІЄH3(ЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБ)ЁЃ
ЁОД№АИЁПP(s)+Cl2(g)=PCl3(g)ЁїH=-306kJ/mol PCl5 (g)= PCl3 (g)+Cl2(g)ЁїH=+93kJ/molЃЛ 399kJ/mol ЕШгк
ЁОНтЮіЁП
ИљОнИЧЫЙЖЈТЩЃЌЗДгІШШгыЭООЖЮоЙиЃЌжЛгыЦ№ЪМЮяжЪЁЂжеСЫЮяжЪгаЙиЃЌвдДЫНтД№БОЬтЁЃ
(1)ВњЮяЕФзмФмСПМѕШЅЗДгІЮяЕФзмФмСПОЭЕШгкЁїHЃЌНсКЯЭМЯѓПЩжЊЃЌPCl3КЭЗДгІЮяPКЭCl2ЕФФмСПВюЮЊ306kJЃЌвђДЫИУШШЛЏбЇЗНГЬЪНЮЊЃКP(s)+Cl2(g)=PCl3(g)ЁїH=-306kJ/molЃЌЙЪД№АИЃКP(s)+Cl2(g)=PCl3(g)ЁїH=-306kJ/molЃЛ
(2)ИљОнЭМЯѓПЩжЊPCl5КЭPCl3ЁЂCl2жЎМфЕФФмСПВюЮЊ-93kJЃЌвђДЫPCl5ЗжНтГЩPCl3КЭCl2ЕФШШЛЏбЇЗНГЬЪНЮЊЃКPCl5 (g)= PCl3 (g)+Cl2(g)ЁїH=+93kJ/molЃЌЙЪД№АИЃКPCl5 (g)= PCl3 (g)+Cl2(g)ЁїH=+93kJ/molЃЛ
(3)ИљОнИЧЫЙЖЈТЩЃКЁїH=-306kJ/mol-93kJ/mol=-399kJ/molЁЃИУЗДгІШШгыЭООЖЮоЙиЃЌжЛгыЦ№ЪМЮяжЪЁЂжеСЫЮяжЪгаЙиЃЌЫљвдPКЭCl2вЛВНЗДгІЩњГЩ1molPCl5ЕФІЄH4ЕШгкІЄH3ЃЌЙЪД№АИЃК399kJ/molЃЛЕШгкЁЃ


 аЁЬьВХПЮЪБзївЕЯЕСаД№АИ
аЁЬьВХПЮЪБзївЕЯЕСаД№АИ вЛПЮЫФСЗЯЕСаД№АИ
вЛПЮЫФСЗЯЕСаД№АИ ЛЦИдаЁзДдЊТњЗжГхДЬЮЂВтбщЯЕСаД№АИ
ЛЦИдаЁзДдЊТњЗжГхДЬЮЂВтбщЯЕСаД№АИ аТИЈНЬЕМбЇЯЕСаД№АИ
аТИЈНЬЕМбЇЯЕСаД№АИ бєЙтЭЌбЇвЛЯпУћЪІШЋгХКУОэЯЕСаД№АИ
бєЙтЭЌбЇвЛЯпУћЪІШЋгХКУОэЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгЭЛЫљгУЕФбеСЯгааэЖрЬьШЛПѓЪЏГЩЗжЃЌПѓЪЏжаЭљЭљКЌгаBЁЂCЁЂOЁЂNaЁЂPЁЂClЕШдЊЫиЃЌЫќУЧдкПЦбЇбаОПКЭЙЄвЕЩњВњжаОпгааэЖргУЭОЁЃЧыЛиД№ЯТСагаЙиЮЪЬтЃК
(1)ЯжДњЛЏбЇжаЃЌГЃРћгУ___ЩЯЕФЬиеїЦзЯпРДМјЖЈдЊЫиЁЃ
(2)![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЖМЪЧживЊЕФгаЛњЗДгІжаМфЬхЁЃ
ЖМЪЧживЊЕФгаЛњЗДгІжаМфЬхЁЃ![]() жаЬМдзгЕФдгЛЏЗНЪНЮЊ_______ЃЌ
жаЬМдзгЕФдгЛЏЗНЪНЮЊ_______ЃЌ![]() ЕФПеМфЙЙаЭЮЊ_____ЁЃ
ЕФПеМфЙЙаЭЮЊ_____ЁЃ
(3)![]() КЭ
КЭ![]() ЛЅЮЊЕШЕчзгЬхЃЌЕчРыФм
ЛЅЮЊЕШЕчзгЬхЃЌЕчРыФм![]() ___
___![]() ЃЈЬюЁА>ЁБЛђЁА<ЁБЃЉЁЃ
ЃЈЬюЁА>ЁБЛђЁА<ЁБЃЉЁЃ
(4)ЙЄвЕЩЯжЦШЁЕЅжЪЗњПЩЭЈЙ§ЕчНт![]() КЭ
КЭ![]() ЕФЛьКЯШмвКЛёЕУЃЌгы
ЕФЛьКЯШмвКЛёЕУЃЌгы![]() ЛЅЮЊЕШЕчзгЬхЕФЗжзгЮЊ_____ЃЈШЮЬювЛжжЃЉЁЃ
ЛЅЮЊЕШЕчзгЬхЕФЗжзгЮЊ_____ЃЈШЮЬювЛжжЃЉЁЃ
(5)ЧтТБЫсЃЈ![]() ЃЉЕФЕчРыЙ§ГЬШчЭМЁЃ
ЃЉЕФЕчРыЙ§ГЬШчЭМЁЃ![]() КЭ
КЭ![]() ЕФЕнБфЙцТЩЖМЪЧ
ЕФЕнБфЙцТЩЖМЪЧ![]() ЃЌЦфжа
ЃЌЦфжа![]() ЬиБ№ДѓЕФдвђЮЊ__________ЃЌДгдзгНсЙЙЗжЮігАЯь
ЬиБ№ДѓЕФдвђЮЊ__________ЃЌДгдзгНсЙЙЗжЮігАЯь![]() ЕнБфЕФвђЫиЮЊ_____ЁЃ
ЕнБфЕФвђЫиЮЊ_____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМЪЧдзгађЪ§ЮЊ1ЁЋ19ЕФдЊЫиЕквЛЕчРыФмЕФБфЛЏЧњЯп(ЦфжаВПЗждЊЫиЕквЛЕчРыФмвбОБъГіЪ§Он)ЁЃНсКЯдЊЫидкдЊЫижмЦкБэжаЕФЮЛжУЃЌЗжЮіЭМжаЧњЯпЕФБфЛЏЬиЕуЃЌВЂЛиД№ЯТСагаЙиЮЪЬтЁЃ
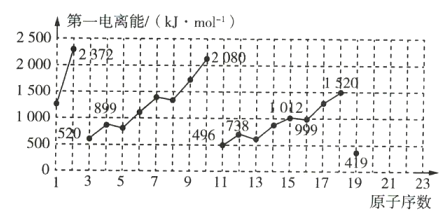
(1)МюН№ЪєдЊЫижаLiЁЂNaЁЂKЕФЕквЛЕчРыФмЗжБ№ЮЊ _____________ ![]() ЁЂ _____________
ЁЂ _____________ ![]() ЁЂ _____________
ЁЂ _____________ ![]() ЁЃ
ЁЃ
(2)ЭЌжїзхжаВЛЭЌдЊЫиЕФЕквЛЕчРыФмБфЛЏЕФЙцТЩЮЊЃК _____________ ЃЌМюН№ЪєдЊЫиетвЛБфЛЏЕФЙцТЩгыМюН№ЪєЕФЛюЦУадЕФЙиЯЕЪЧ _____________ ЁЃ
(3)ИЦдЊЫиЕФЕквЛЕчРыФмЕФЪ§жЕЗЖЮЇЮЊ _____________ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЃКЃЈ1ЃЉH2(g)ЃЋ![]() O2(g)=H2O(g) ІЄH1=akJЁЄmol-1
O2(g)=H2O(g) ІЄH1=akJЁЄmol-1
ЃЈ2ЃЉ2H2(g)ЃЋO2(g)=2H2O(g) ІЄH2=bkJЁЄmol-1
ЃЈ3ЃЉH2(g)ЃЋ![]() O2(g)=H2O(l) ІЄH3=ckJЁЄmol-1
O2(g)=H2O(l) ІЄH3=ckJЁЄmol-1
ЃЈ4ЃЉ2H2(g)ЃЋO2(g)=2H2O(l) ІЄH4=dkJЁЄmol-1ЃЛЯТСаЙиЯЕЪНжае§ШЗЕФЪЧЃЈ ЃЉ
A.a<c<0B.2a=b<0C.b>d>0D.2c=d>0
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкУмБеШнЦїжаЗЂЩњЗДгІЃКxA(g)+yB(g)![]() zC(g)ЃЌЦНКтЪБВтЕУAЕФХЈЖШЮЊ0.50mol/LЃЌБЃГжЮТЖШВЛБфЃЌНЋШнЦїЕФШнЛ§РЉДѓЕНдРДЕФСНБЖЃЌдйДяЦНКтЪБЃЌВтЕУAЕФХЈЖШ0.30mol/LЁЃЯТСагаЙиХаЖЯе§ШЗЕФЪЧЃЈ ЃЉ
zC(g)ЃЌЦНКтЪБВтЕУAЕФХЈЖШЮЊ0.50mol/LЃЌБЃГжЮТЖШВЛБфЃЌНЋШнЦїЕФШнЛ§РЉДѓЕНдРДЕФСНБЖЃЌдйДяЦНКтЪБЃЌВтЕУAЕФХЈЖШ0.30mol/LЁЃЯТСагаЙиХаЖЯе§ШЗЕФЪЧЃЈ ЃЉ
A.x+y<z
B.ЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ
C.AЕФзЊЛЏТЪНЕЕЭ
D.CЕФЬхЛ§ЗжЪ§діДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЬхЛ§ЕФУмБеШнЦїжаЃЌНјааШчЯТЛЏбЇЗДгІЃКCO2(g)ЃЋH2(g) ![]() CO(g)ЃЋH2O(g)ЃЌЦфЛЏбЇЦНКтГЃЪ§KКЭЮТЖШtЕФЙиЯЕШчЯТБэЫљЪОЃК
CO(g)ЃЋH2O(g)ЃЌЦфЛЏбЇЦНКтГЃЪ§KКЭЮТЖШtЕФЙиЯЕШчЯТБэЫљЪОЃК
t Ёц | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉИУЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊKЃН_________________________________ЁЃ
ЃЈ2ЃЉИУЗДгІЮЊ________ЗДгІ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЁЃ
ЃЈ3ЃЉФГЮТЖШЯТЃЌИїЮяжЪЕФЦНКтХЈЖШЗћКЯЯТЪНЃК3c(CO2)ЁЄc(H2)ЃН5c(CO)ЁЄc(H2O)ЃЌЪдХаЖЯДЫЪБЕФЮТЖШЮЊ______ЁЃ
ЃЈ4ЃЉШє830 ЁцЪБЃЌЯђШнЦїжаГфШы1 mol COЁЂ5 mol H2OЃЌЗДгІДяЕНЦНКтКѓЃЌЦфЛЏбЇЦНКтГЃЪ§K______1.0(ЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБ)ЁЃ
ЃЈ5ЃЉ830 ЁцЪБЃЌШнЦїжаЕФЗДгІвбДяЕНЦНКтЁЃдкЦфЫћЬѕМўВЛБфЕФЧщПіЯТЃЌРЉДѓШнЦїЕФЬхЛ§ЁЃЦНКт____вЦЖЏ(ЬюЁАЯђе§ЗДгІЗНЯђЁБЁАЯђФцЗДгІЗНЯђЁБЛђЁАВЛЁБ)ЁЃ
ЃЈ6ЃЉШє1 200 ЁцЪБЃЌдкФГЪБПЬЦНКтЬхЯЕжаCO2ЁЂH2ЁЂCOЁЂH2OЕФХЈЖШЗжБ№ЮЊ2 molЁЄLЃ1ЁЂ2 molЁЄLЃ1ЁЂ4 molЁЄLЃ1ЁЂ4 molЁЄLЃ1ЃЌдђДЫЪБЩЯЪіЗДгІЕФЦНКтвЦЖЏЗНЯђЮЊ__________(ЬюЁАе§ЗДгІЗНЯђЁБЁАФцЗДгІЗНЯђЁБЛђЁАВЛвЦЖЏЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
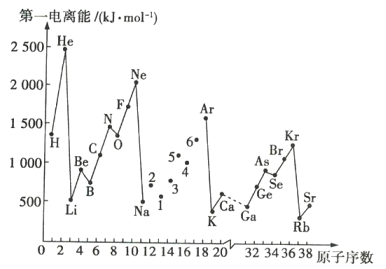
ЁОЬтФПЁПЕквЛЕчРыФмЪЧжИДІгкЛљЬЌЕФЦјЬЌдзгЪЇШЅвЛИіЕчзгЃЌЩњГЩ+1МлЦјЬЌбєРызгЫљашвЊЕФФмСПЁЃШчЭМЪЧВПЗждЊЫиЕФЕквЛЕчРыФмI1ЫцдзгађЪ§БфЛЏЕФЧњЯпЭМЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЗжЮіЭМжаЭЌжмЦкдЊЫиЕквЛЕчРыФмЕФБфЛЏЙцТЩЃЌНЋNaЁЋArжЎМф1~6КХдЊЫигУЖЬЯпСЌНгЦ№РДЃЌЙЙГЩЭъећЕФЭМЯѓ___ЁЃ
ЃЈ2ЃЉИљОнЭМЗжЮіПЩжЊЃЌЭЌжїзхдЊЫиЕФЕквЛЕчРыФмЕФБфЛЏЙцТЩЪЧ___ЁЃ
ЃЈ3ЃЉЭМжа5КХдЊЫидкдЊЫижмЦкБэжаЕФЮЛжУЪЧ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖЬжмЦкжїзхдЊЫи WЁЂXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌW дкДѓЦјжагаСНжжЭЌЫивьаЮЬхЧвОљФмжЇГжШМЩеЃЌX ЕФдзгАыОЖЪЧЫљгаЖЬжмЦкжїзхдЊЫижазюДѓЕФЃЌЗЧН№ЪєдЊЫи Y ЕФд згађЪ§ЪЧ Z ЕФзюЭтВуЕчзгЪ§ЕФ 2 БЖЁЃЯТСаа№ЪіВЛе§ШЗЕФЪЧ
A.YЁЂZЕФЧтЛЏЮяЮШЖЈад Y> Z
B.YЕЅжЪЕФШлЕуИпгкX ЕЅжЪ
C.XЁЂWЁЂZ ФмаЮГЩОпгаЧПбѕЛЏадЕФ XZW
D.YZ4Зжзгжа Y КЭ Z ЖМ Тњзу8 ЕчзгЮШЖЈНсЙЙ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
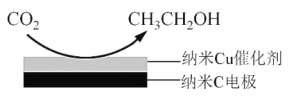
ЁОЬтФПЁПЪЎОХДѓБЈИцЬсГівЊЖдЛЗОГЮЪЬтНјааШЋУцЁЂЯЕЭГЕФПЩГжајжЮРэЁЃТЬЩЋФмдДЪЧЪЕЪЉПЩГжајЗЂеЙ ЕФживЊЭООЖЃЌРћгУЩњЮяввДМРДжЦШЁТЬЩЋФмдДЧтЦјЕФВПЗжЗДгІЙ§ГЬШчЭМЫљЪОЃК
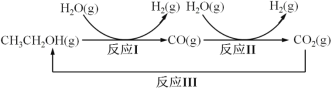
ЃЈ1ЃЉвбжЊЃКCO(g)+H2O(g) ![]() CO2(g)+H2(g) ЁїH1= - 41 kJ/mol
CO2(g)+H2(g) ЁїH1= - 41 kJ/mol
CH3CH2OH(g)+3H2O(g) ![]() 2CO2(g)+6H2(g) ЁїH2=+174.1 kJ/mol
2CO2(g)+6H2(g) ЁїH2=+174.1 kJ/mol
ЧыаДГіЗДгІ I ЕФШШЛЏбЇЗНГЬЪН____________ЁЃ
ЃЈ2ЃЉЗДгІ IIЃЌдкНјЦјБШ[n(CO) : n(H2O)]ВЛЭЌЪБЃЌВтЕУЯргІЕФ CO ЦНКтзЊЛЏТЪМћЭМЃЈИїЕуЖдгІЕФЗДгІЮТЖШПЩФмЯрЭЌЃЌвВПЩФмВЛЭЌЃЛИїЕуЖдгІЕФЦфЫћЗДгІЬѕМўЖМЯрЭЌЃЉЁЃ

ЂйОЗжЮіЃЌAЁЂE КЭ G Ш§ЕуЖдгІЕФЗДгІЮТЖШЯрЭЌЃЌЦфдвђЪЧ KA=KE=KG=____________ЃЈЬюЪ§жЕЃЉЁЃдкИУЮТЖШЯТЃКвЊЬсИп COЦНКтзЊЛЏТЪЃЌГ§СЫИФБфНјЦјБШжЎЭтЃЌЛЙПЩВЩШЁЕФДыЪЉЪЧ____________ЁЃ
Ђк ЖдБШЗжЮі BЁЂEЁЂF Ш§ЕуЃЌПЩЕУГіЖдгІЕФНјЦјБШКЭЗДгІЮТЖШЕФБфЛЏЧїЪЦжЎМфЕФЙиЯЕЪЧ____________ЁЃ
Ђл БШНЯ AЁЂB СНЕуЖдгІЕФЗДгІЫйТЪДѓаЁЃКVA____________VBЃЈЬюЁА<ЁБ ЁА=ЁБЛђЁА>ЁБЃЉЁЃвбжЊЗДгІЫйТЪ v=v е§v Фц= kе§XЃЈCOЃЉXЃЈH2OЃЉЃkФцXЃЈCO2ЃЉXЃЈH2ЃЉЃЌk е§ЁЂk ФцЗжБ№ЮЊе§ЁЂФцЯђЗДгІЫйТЪГЃЪ§ЃЌXЮЊЮяжЪЕФСПЗжЪ§МЦЫудкДяЕНЦНКтзДЬЌЮЊDЕуЕФЗДгІЙ§ГЬжаЃЌЕБCOзЊЛЏТЪИеКУДяЕН20%ЪБЃЌ![]() =_____________ЃЈМЦЫуНсЙћБЃСє1ЮЛаЁЪ§ЃЉЁЃ
=_____________ЃЈМЦЫуНсЙћБЃСє1ЮЛаЁЪ§ЃЉЁЃ
ЃЈ3ЃЉЗДгІ III РћгУЬМЫсМиШмвКЮќЪе CO2 ЕУЕНБЅКЭ KHCO3 ЕчНтвКЃЌЕчНтЛюЛЏЕФ CO2 РДжЦБИввДМЁЃ
ЂйвбжЊЬМЫсЕФЕчРыГЃЪ§ Ka1=10-a molЁЄL1ЃЌKa2=10-b molЁЄL1ЃЌЮќЪезуСП CO2 ЫљЕУБЅКЭ KHCO3 ШмвКЕФ pH=cЃЌдђИУШмвКжаlg![]() =________________
=________________
ЂкдкБЅКЭ KHCO3 ЕчНтвКжаЕчНт CO2 РДжЦБИввДМЕФдРэШчЭМЫљЪОЁЃдђвѕМЋЕФЕчМЋЗДгІЪНЪЧ__________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com