
【题目】发射卫星的火箭推进器中大多使用燃料偏二甲肼,其化学式C2H8N2。
计算:(1)偏二甲肼的摩尔质量是________;480 g偏二甲肼的物质的量为 ________。
(2)偏二甲肼中碳原子与氮原子的个数之比是________,其物质的量之比是 ________;1mol偏二甲肼中含有的氢原子数目是________。
【答案】60g/mol8mol1:11:18NA
【解析】
(1)摩尔质量以g/mol为单位,数值上等于其相对分子质量,根据n=![]() 计算480g偏二甲肼的物质的量;
计算480g偏二甲肼的物质的量;
(2)根据化学式确定偏二甲肼中碳原子与氮原子的个数之比、物质的量之比;H原子物质的量为偏二甲肼的8倍,再根据N=nNA计算H原子数目。
(1) C2H8N2的相对分子质量为60,故其摩尔质量为60g/mol,480g偏二甲肼的物质的量为![]() =8mol,
=8mol,
因此,本题正确答案是:60g/mol;8mol;
(2)根据偏二甲肼化学式C2H8N2,可以知道碳原子与氮原子的个数之比2:2=1:1、C、N原子物质的量之比为1:1;H原子物质的量为偏二甲肼的8倍,1mol偏二甲肼含有H原子数目1mol![]() 8
8![]() NAmol-1=8NA,
NAmol-1=8NA,
因此,本题正确答案是:1:1 ;1:1;8NA。


 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
【题目】肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图1。已知200℃时:
反应 I : 3N2H4(g)=N2(g)+4NH3(g) △Hl=-32.9kJ/mol
反应II: N2H4(g)+H2(g)=2NH3(g) △H2=-41.8 kJ/mol

下列说法不正确的是
A. 图l所示过程①、②都是放热反应
B. 反应Ⅱ的能量过程示意图如图2所示
C. 断开3 molN2H4(g)中的化学键吸收的能量大于形成1 molN2(g)和4 molNH3(g)中的化学键释放的能量
D. 200℃时,肼分解生成氨气和氢气的热化学方程式为N2H4(g) =N2(g)+2H2 (g) △H=+50.7 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。很多鲜花和水果的香味都来自酯的混合物。现在可以通过人工方法合成各种酯,用作饮料、糖果、香水、化妆品中的香料,也可以用作指甲油、胶水的溶剂。下图是工业上以A为主要原料来合成乙酸乙酯的合成路线。其中A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工发展水平。又知2CH3CHO+O2![]() 2CH3COOH。请回答下列问题
2CH3COOH。请回答下列问题
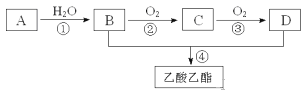
(1)B、D分子内含有的官能团分别是_________、_________(填名称)。
(2)写出下列反应的反应类型:①______________,④______________。
(3)写出下列反应的化学方程式:
②_______________________________________________________;
④____________________________________________________。
(3)A与H2在催化剂作用下充分反应生成E,E的同系物F比E多三个碳原子,请写出F的所有同分异构体的结构简式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】提纯下列物质除去其中的杂质(括号中为杂质),所用试剂和方法正确的是( )
A.H2SO4(HCl):AgNO3溶液、过滤
B.KNO3(K2SO4):Ba(NO3)2溶液、过滤
C.Cu(CuO):盐酸、过滤
D.CaCO3(CaO):水、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(乙二酸)存在于自然界的植物中,易挥发,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水,草酸晶体(H2C2O4 · 2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解,回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是_____,由此可知草酸晶体分解的产物中有_____,装置B的主要作用是_____。

(2)乙组同学认为草酸晶体分解产物中还有CO,为进行验证,选用甲组实验中的装置A、B和下图所示的部分装置(可重复选用)进行实验。


①乙组同学的实验装置中,依次连接的合理顺序为A、B、_____,装置H中装有的物质是_____。
②能证明草酸晶体分解产物中有CO的现象是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有x g某气体,它由三原子分子构成,它的摩尔质量为M gmol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体所含原子总数为_____个。
(2)该气体在标准状况下的体积为______L。
(3)一个该气体分子的质量______g。
Ⅱ.(1)等物质的量的CO和CO2其原子数之比为 ______。
(2)同温、同压下,A、B两容器分别充满O2和O3 ,则O2和O3的密度之比为______,若两容器中O2和O3 所含原子总数相等,则A容器和B容器的容积比是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋![]() 主要成分
主要成分![]() 、纯碱
、纯碱![]() 和小苏打
和小苏打![]() 均为家庭厨房中常用的物质
均为家庭厨房中常用的物质![]() 己知:
己知:
弱酸 |
|
|
|
电离常数 |
|
|
|
请回答下列问题:
(1)![]() 时,
时, ![]() 溶液的
溶液的![]() ,则溶液中由水电离出的
,则溶液中由水电离出的![]() ______ mol/L。
______ mol/L。
(2)常温下,将![]() 溶液和
溶液和![]() 溶液分别与20mL
溶液分别与20mL![]() 溶液混合
溶液混合![]() 混合后溶液体积变化忽略不计
混合后溶液体积变化忽略不计![]() .
.
①反应开始时,v ![]()
![]() ______ v
______ v![]() 填“
填“![]() ”、“
”、“![]() ”或“:”
”或“:”![]() .
.
②充分反应后![]() 两溶液中
两溶液中![]() ______
______ ![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
” ![]() .
.
(3)![]() 时,向
时,向![]() 溶液中加入一定量的
溶液中加入一定量的![]() ,所得混合液的
,所得混合液的![]() ,则混合液中
,则混合液中 ______ ;
______ ;
(4)常温下,下列方法可以使![]() 的电离程度增大的是 ______ .
的电离程度增大的是 ______ .
![]() 加入少量的稀盐酸
加入少量的稀盐酸 ![]() 加热溶液
加热溶液
![]() 加水稀释
加水稀释 ![]() 加入少量冰醋酸.
加入少量冰醋酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示不同化学元素所组成的化合物,以下说法不正确的是

A. 若图中①为某种多聚体的单体,则①最可能是氨基酸
B. 若②存在于皮下和内脏器官周围等部位,则②不仅是储能物质,还有保温的作用
C. 若③为多聚体,且能贮存生物的遗传信息,则③是DNA
D. 若④主要在人体肝脏和肌肉内合成,则④最可能是糖原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com