
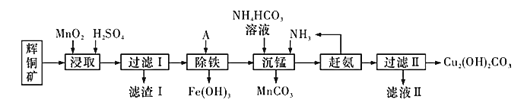
【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如图:
(1)加快“浸取”速率除将辉铜矿粉碎外,还可采取的措施有_________ (任写一种);研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是________。
(2)滤渣I中的主要成分是MnO2、S、SiO2。请写出“浸取”反应中生成S的化学方程式:________。
(3)常温下“除铁”时加入的试剂A可用____________较为合适,若加A后溶液的pH调为5,则溶液中Fe3+ 的浓度为______mol/L。{Ksp[Fe(OH)3]=4.0×10- 38}
(4)写出“沉锰"(除Mn2+ )过程中反应的离子方程式:______。
(5)“赶氨”时,最适宜的操作方法是__________。
(6)滤液II经蒸发结晶得到的盐主要是________(写化学式)。
【答案】适当提高硫酸的浓度或适当加热或充分搅拌 Fe3+可催化Cu2S被MnO2氧化 2MnO2+Cu2S+4H2SO4=S↓+ 2CuSO4+2MnSO4+4H2O CuO ![]() Mn2++HCO3-+NH3=MnCO3↓+NH4+ 将溶液加热 (NH4)2SO4
Mn2++HCO3-+NH3=MnCO3↓+NH4+ 将溶液加热 (NH4)2SO4
【解析】
辉铜矿主要成分为Cu2S,含少量Fe2O3、SiO2等杂质,加入稀硫酸和二氧化锰浸取,过滤得到滤渣为为二氧化锰、二氧化硅和单质硫,滤液中含有铁离子、锰离子和铜离子,调节溶液pH除去铁离子,加入碳酸氢铵溶液沉淀锰,过滤得到滤液,赶出氨气循环使用,得到碱式碳酸铜。
(1)加快“浸取”速率除将辉铜矿粉碎外,还可以适当提高硫酸的浓度、适当加热、充分搅拌等,浸取时,Fe2O3和稀硫酸反应生成硫酸铁和水,Fe2O3起媒介作用,Fe3+可催化Cu2S被MnO2氧化,若先除铁再浸取,浸取速率明显变慢,故答案为:适当提高硫酸的浓度或适当加热或充分搅拌;Fe3+可催化Cu2S被MnO2氧化;
(2)滤渣I中的主要成分是MnO2、S、SiO2。“浸取”反应中生成S的化学方程式为:2MnO2+Cu2S+4H2SO4=S↓+ 2CuSO4+2MnSO4+4H2O,故答案为:2MnO2+Cu2S+4H2SO4=S↓+ 2CuSO4+2MnSO4+4H2O;
(3)常温下“除铁”时加入的试剂A可用CuO较为合适,已知Ksp[Fe(OH)3]=4.0×10- 38,pH=5,则c(H+)=10-5,c(OH-)=10-9,Ksp[Fe(OH)3]=![]() 4.0×10- 38,
4.0×10- 38,![]() mol/L,故答案为:CuO;
mol/L,故答案为:CuO;![]() ;
;
(4)“沉锰"过程中加入碳酸氢铵和氨气,生成碳酸锰,其离子方程式为:Mn2++HCO3-+NH3=MnCO3↓+NH4+,故答案为:Mn2++HCO3-+NH3=MnCO3↓+NH4+;
(5)“赶氨”时,最适宜的操作方法是减小氨气溶解度,氨气是易挥发性气体,加热驱赶,故答案为:将溶液加热;
(6)滤液II主要是硫酸铵溶液,通过蒸发浓缩、冷却结晶、过滤洗涤得到硫酸铵晶体,故答案为:(NH4)2SO4。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.pH=l的溶液中:Ba2+、Fe3+、Cl-、SCN-
B.能使酚酞变红的溶液:Ca2+、K+、HCO3-、CO32-
C.![]() =10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
=10-12的溶液中:NH4+、Cu2+、NO3-、SO42-
D.由水电离的c(H+)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国对二氧化硫一空气质子交换膜燃料电池的研究处于世界前沿水平,该电池可实现硫酸生产、发电和环境保护三位一.体的结合。其原理如图所示。下列说法不正确的是( )
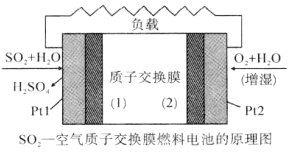
A.Pt1电极附近发生的反应为:SO2+2H2O-2e-=H2SO4+2H+
B.相同条件下,放电过程中消耗的SO2和O2的体积比为2:1
C.该电池工作时质子从Pt1电极经过内电路流到Pt2电极
D.该电池实现了制硫酸、发电、环保三位一体的结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在-50℃时液氨中存在着下列平衡:2NH3(液)![]() NH4++NH2-,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时离子积的叙述中正确的是( )
NH4++NH2-,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时离子积的叙述中正确的是( )
A. 离子积为1.0×10-15
B. 离子积为1.0×10-30
C. 向液氨中加入氨基钠(NaNH2),液氨的离子积增大
D. 向液氨中加入NH4Cl,c(NH4+)增大,离子积的数值也随之增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个定容的密闭容器中进行如下反应:2SO2(g)+O2(g) ![]() 2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为0.1 mol·L-1、0.05 mol·L-1和0.3 mol·L-1。当反应达平衡时不可能存在的数据正确的是
2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为0.1 mol·L-1、0.05 mol·L-1和0.3 mol·L-1。当反应达平衡时不可能存在的数据正确的是
A. c(SO2)=0.25 mol·L-1 B. c(O2)=0.12 mol·L-1
C. c(SO2)+c(SO3)=0.15 mol·L-1 D. c(SO3)+c(O2)=0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛(![]() ),杏仁含苯甲醛(
),杏仁含苯甲醛(![]() )。则下列说法中错误的是( )
)。则下列说法中错误的是( )
A.肉桂醛和苯甲醛互为同系物
B.苯甲醛分子中所有原子可能位于同一平面内
C.肉桂醛能发生加成反应、取代反应和加聚反应
D.与肉桂醛互为同分异构体且含相同官能团和苯环结构的共有4种(不考虑顺反异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述正确的是( )
A.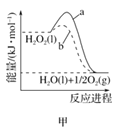 图甲表示H2O2在有、无催化剂下的分解反应能量变化曲线,b表示有催化剂时的反应
图甲表示H2O2在有、无催化剂下的分解反应能量变化曲线,b表示有催化剂时的反应
B.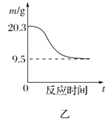 图乙表示0.1molMgCl26H2O在空气中充分加热时固体质量随时间的变化
图乙表示0.1molMgCl26H2O在空气中充分加热时固体质量随时间的变化
C.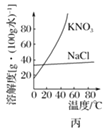 图丙表示KNO3和NaCl的溶解度曲线,若欲除去NaCl中少量KNO3,可将混合物制成较高温度下的浓溶液再冷却结晶、过滤
图丙表示KNO3和NaCl的溶解度曲线,若欲除去NaCl中少量KNO3,可将混合物制成较高温度下的浓溶液再冷却结晶、过滤
D.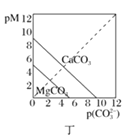 图丁表示碳酸盐的溶解平衡曲线[pM=-lgc(M),p(CO32-)=-lgc(CO32-)],则Ksp(CaCO3)>Ksp(MgCO3)
图丁表示碳酸盐的溶解平衡曲线[pM=-lgc(M),p(CO32-)=-lgc(CO32-)],则Ksp(CaCO3)>Ksp(MgCO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莫尔法是用硝酸银标准溶液测定卤离子含量的沉淀滴定法。某实验兴趣小组将无水FeCl3与氯苯混合发生反应:2FeCl3 +C6H5Cl![]() 2FeCl2 +C6H4Cl2+HC1↑,将生成的HCl用水吸收,利用莫尔法测出无水FeCl3的转化率,同时得到常用的还原剂FeCl2。按照如图装置:
2FeCl2 +C6H4Cl2+HC1↑,将生成的HCl用水吸收,利用莫尔法测出无水FeCl3的转化率,同时得到常用的还原剂FeCl2。按照如图装置:
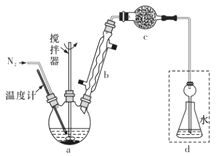
在三颈烧瓶中放入162.5g无水FeCl3与225 g氯苯,控制反应温度在130℃下加热3 h,冷却、过滤,洗涤、干燥得到粗产品。有关数据如表:
C6H5Cl | C6H4Cl2 | AgCl | Ag2CrO4 | |
颜色 | — | — | 白色 | 砖红色 |
溶度积 | — | — | 1.56×10-10 | 9×10-12 |
熔点/℃ | -45 | 53 | — | — |
沸点/℃ | 132 | 173 | — | — |
回答下列问题:
(1)仪器c的名称是_______,盛装的试剂可以是_______________(填字母代号)。
A.碱石灰 B,浓硫酸 C.无水氯化钙 D.固体氢氧化钠
(2)下列各装置(盛有蒸馏水)能代替图中虚线框内部分的是______(填字母代号)。
e.  f.
f.  g.
g. 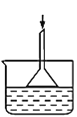 h.
h. 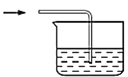
(3)如何从滤液中回收过量的氯苯:__________。
(4)将锥形瓶内的溶液稀释至1 000 mL,从中取出10. 00 mL,滴加几滴K2CrO4 作指示剂,用0. 200 0 mol/L AgNO3溶液进行滴定,当达到终点时平均消耗22. 50 mL AgNO3溶液。
①滴定终点的现象是________,使用棕色滴定管进行滴定的目的是_________。
②无水FeCl3的转化率α=_______
③上述滴定完成时,若滴定管尖嘴处留有气泡会导致测定结果偏________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会、生活密切相关。下列说法错误的是( )
A.蚕丝属于天然高分子材料
B.雾霾纪录片《穹顶之下》,提醒人们必须十分重视环境问题,提倡资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle)
C.化石燃料完全燃烧不会造成大气污染
D.中国古代用明矾溶液清洗铜镜表面的铜锈
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com