
| A. | 在接触室里用98.3%的浓硫酸吸收SO3,目的是防止形成酸雾便于SO3吸收完全 | |
| B. | 工业制玻璃和炼铁过程中都要加入石灰石,目的是除去杂质二氧化硅 | |
| C. | 工业上用金属钠与TiCl4溶液在高温下反应,目的是将金属钛从氯化物中置换出来 | |
| D. | 海水中提取镁的过程中加入贝壳煅烧制得的石灰,目的是将Mg2+转变成Mg(OH)2 |
分析 A.若用水或稀硫酸吸收,易形成酸雾,且吸收速度慢;
B.炼铁材料为铁矿石、焦炭、石灰石,加入石灰石,目的是除去杂质二氧化硅,生产普通玻璃的原料有砂子,石灰石和纯碱;
C.工业上生产钛是在高温下用熔融TiCl4与钠反应制得;
D.把贝壳制成石灰乳[Ca(OH)2],发生的反应为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、CaO+H2O=Ca(OH)2,在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,发生的反应为Mg2++2OH-=Mg(OH)2↓;
解答 解:A.在吸收塔中三氧化硫与水反应生成硫酸,但水直接吸收三氧化硫会形成酸雾,使三氧化硫的吸收率降低,生产实践中用98.3%的浓H2SO4吸收三氧化硫,可以防止形成酸雾,使SO3吸收完全,故A正确;
B.炼铁材料为铁矿石、焦炭、石灰石,加入石灰石,目的是除去杂质二氧化硅,普通玻璃的原料有砂子,石灰石和纯碱,石灰石是制玻璃的原料之一,故B错误;
C.工业上生产钛是在高温下用熔融TiCl4与钠反应制得,钠与TiCl4溶液在高温下不能置换出钛,故C错误;
D.把贝壳制成石灰乳[Ca(OH)2],发生的反应为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑、CaO+H2O=Ca(OH)2,在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,发生的反应为Mg2++2OH-=Mg(OH)2↓,所以加入贝壳煅烧制得的石灰,目的是将Mg2+转变成Mg(OH)2,故D正确;
故选AD.
点评 本题考查了硫酸的制备、工业制玻璃和炼铁的原理、钛以及镁的制备等,属于对基础知识的考查,注意金属冶炼方法与其活泼性强弱的关系,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | NH3是氧化剂 | B. | H2O是氧化产物 | ||
| C. | NO2发生氧化反应 | D. | 生成1mol H2O转移2mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 现象或反应 | 原理解释 | |
| A | 氯化铵溶液可以除去铁器表面的铁锈 | 氯化铵水解,溶液显酸性 |
| B | 合成氨反应需在高温条件下进行 | 该反应为吸热反应 |
| C | 镀层破损后,镀锌铁仍不易腐蚀 | 活泼性锌强于铁 |
| D | 2CO=2C+O2在任何温度下均不能自发进行 | 该反应△H>0,△S<0 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生石灰-Ca(OH)2 | B. | 重晶石-BaCO3 | C. | 明矾-CuSO4•5H2O | D. | 小苏打-NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.16 moL•L-1 | B. | 0.08 moL•L-1 | C. | 0.04moL•L-1 | D. | 0.02moL•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
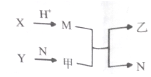 短周期元素A、B、C、D的原子序数依次增加.X、Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两元素对应的单质.若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )
短周期元素A、B、C、D的原子序数依次增加.X、Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、乙为其中两元素对应的单质.若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如图所示(部分反应物或生成物省略),则下列说法中正确的是( )| A. | 相对分子质量M>N,沸点N>M | |
| B. | 常温常压下B的氢化物为气体,C的氢化物为固体 | |
| C. | 原子半径:D>B>C>A | |
| D. | D的最高价氧化物的水合物为强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com