
NaHCO3和NaHSO4的溶液混合后,实际参加反应的离子是( )
A.H+和CO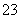 B.HCO
B.HCO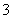 和HSO
和HSO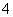
C.Na+、HCO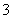 和H+ D.HCO
和H+ D.HCO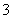 和H+
和H+
科目:高中化学 来源: 题型:

观察1s轨道电子云示意图,判断下列说法正确的是( )
A.一个小黑点表示1个自由运动的电子
B.1s轨道的电子云形状为圆形的面
C.电子在1s轨道上运动像地球围绕太阳旋转
D.1s轨道电子云中点的疏密表示电子在某一位置出现机会的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中加入A和B,各物质的物质的量浓度随着反
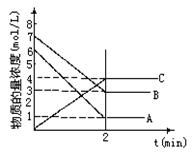
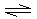 应的进行,如右图所示。下列说法不正确的是
应的进行,如右图所示。下列说法不正确的是
A.该反应的化学方程式为5A+4B 4C
B.2min时,该反应达到平衡,此时A、B、C的浓度
比为5:4:4
C.用B的浓度变化表示2min内的速率为
2mol/(L·min)
D.2min前,正反应速率逐渐减小,逆反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO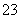
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO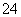
C.加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH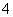
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
关于某无色透明溶液,下列说法正确的是( )
A.若向其中加入铝粉能产生氢气,则NH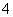 、NO
、NO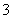 、SO
、SO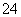 、MnO
、MnO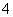 一定不可能共存于溶液
一定不可能共存于溶液
B.若溶液中含有大量Al3+,则溶液中还可能含有Mg2+、SO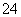 、HCO
、HCO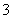
C.若溶液中水电离产生的[H+]=1×10-13 mol·L-1,则S2-、,SO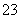 、NH
、NH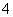 、K+可能存在于溶液中
、K+可能存在于溶液中
D.若溶液能使pH试纸变红,则溶液中I-、Mg2+、NO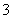 、Cl-可能存在
、Cl-可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
下列排列顺序正确的是:( )
A.微粒半径:Na+>K+>Cl->S2- B.稳定性:HI> HBr>HCl>HF
C.酸性: HClO4>H2SO4>H3PO4>H2SiO4 D.熔点: Al > Mg > Na > K
查看答案和解析>>
科目:高中化学 来源: 题型:
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
②3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
③Fe3O4(s)+CO(g)==3FeO(s)+ CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
下表给出14—17号元素的一些性质,请回答:
| 14Si | 15P | 16S | 17Cl | |
| 单质与H2 反应的条件 | 高温 | 磷蒸气与 H2能反应 | 加热 | 光照或点燃 时发生爆炸 |
| 最高价氧化 物的水化物 | H4SiO4 弱酸 | H3PO4 中强酸 | H2SO4 强酸 | HClO4 最强含氧酸 |
(1)它们所形成的氢化物中稳定性最差的是 ,还原性最差的是 。
(2)四种元素的非金属性随着元素原子序数的递增而逐渐 ,试从原子结构的角度加以解释
。
(3)一定条件下,反应H2S+Cl2=2HCl+S能否发生?简述理由。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com