
【题目】某元素原子的原子核外有三个电子层,最外层电子数是4,该原子核内的质子数是( )
A. 14B. 15C. 16D. 17
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列分子中的中心原子杂化轨道的类型相同的是( )
A. CO2与SO2 B. CH4与NH3 C. BeCl2与BF3 D. C2H2与C2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子的性质的解释中,不正确的是( )
A. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B. 酸性:H3PO4>HClO,因为 H3PO4 的非羟基氧原子数比 HClO 的多
C. 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致
D. 青蒿素分子式为 C15H22O5,结构见图,该分子中包含 7 个手性碳原子

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuS、Cu2S用于处理酸性废水中的Cr2O72-反应如下。反应I:CuS+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平) 反应Ⅱ:Cu2S+Cr2O72-+H+→Cu2++SO42-+Cr3++H2O(未配平) 下列有关说法正确的是
A. 反应I和Ⅱ中各有2种元素的化合价发生变化
B. 处理1molCr2O72-时反应I、Ⅱ中消耗H+的物质的量相等
C. 反应Ⅱ中还原剂与氧化剂的物质的量之比为3:5
D. 质量相同时,Cu2S能去除更多的Cr2O72-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾常用作消毒杀菌、水质净化剂等。某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题。

(1)配平焙烧时化学反应: □MnO2+□_____+□O2![]() □K2MnO4+□H2O;__________
□K2MnO4+□H2O;__________
(2)滤渣II的成分有_______(化学式);第一次通CO2不能用稀盐酸代替的原因是_________。
(3)第二次通入过量CO2生成MnO2的离子方程式为_________。
(4)将滤液Ⅲ进行一系列操作得KMnO4。由下图可知,从滤液Ⅲ得到KMnO4需经过_____、______、洗涤等操作。

(5)工业上按上述流程连续生产。含MnO2a%的软锰矿1吨,理论上最多可制KMnO4___吨。
(6)利用电解法可得到更纯的KMnO4。用惰性电极电解滤液II。
①电解槽阳极反应式为____________;
②阳极还可能有气体产生,该气体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有六种元素,其中 A、B、C、D 为短周期主族元素,E、F 为第四周期元素,它们的原子序数依次增大。
A 元素原子的核外 p 电子数比 s 电子数少 3 |
B 元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
C 元素基态原子 p 轨道有 3 个未成对电子 |
D 原子核外所有 p 轨道全满或半满 |
E 在该周期中未成对电子数最多 |
F 能形成红色(或砖红色)和黑色的两种氧化物 |
请根据以上相关信息,回答问题:
(1)A 的卤化物在工业中有重要作用,A 的四种卤化物的沸点如下表所示:
卤化物 | AF3 | ACl3 | ABr3 | AI3 |
沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是_________________。
② ACl3、LiAH4 中A 原子的杂化轨道类型依次为______、_______;与 A3N3H6 互为等电子体的分子的结构简式为___________。
③用AF3分子结构解释反应 AF3(g)+NH4F(s)=NH4AF4(s)能够发生的原因:_________________。
(2)某同学根据上述信息,推断
①B基态原子的核外最子排布为 ,该同学所画的电子排布图违背了________。
,该同学所画的电子排布图违背了________。
② 已知元素 B 的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是________。
A.分子中含有分子间氢键 B.属于含有极性键的非极性分子
C.只含有4个sp-s的σ键和1个p-p的π键 D.该氢化物分子中 B 原子采用 sp2 杂化
(3)D 基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈______形。
(4)写出 E 原子的电子排布式______________。
(5)请写出 F 元素外围电子排布式_________。向 FSO4溶液中滴加入C元素氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,请写出沉淀溶解的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】洛索洛芬钠可用于类风湿性关节炎、肩周炎等炎症的消炎,其合成路线如下:

已知:A分子式为C8H8,E的分子式为C4H6
i.![]()
ii.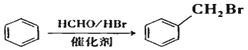
iii.
(1)A属于芳香烃,其名称为_____________。
(2)反应②的反应类型是____________________。
(3)B的结构简式是_________________________。
(4)D中含有的官能团名称____________。
(5)反应①的化学方程式是__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组拟用下图装置进行钠与氧气反应的实验。

(1)将一小块钠放在石棉网上加热,能观察到的实验现象有______________________, 写出发生反应的化学方程式:________________。
(2)上述实验中还观察到有黑色固体物质生成,其原因可能为2Na+CO2![]() C+Na2O2或4Na+3CO2
C+Na2O2或4Na+3CO2![]() C+2Na2CO3,这两个化学方程式的反应类型既属于基本反应类型中的__________反应,也属于__________(填“氧化还原”或“非氧化还原”)反应。
C+2Na2CO3,这两个化学方程式的反应类型既属于基本反应类型中的__________反应,也属于__________(填“氧化还原”或“非氧化还原”)反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com