
| A. | 参加反应的CO2的体积为0.224 a L | |
| B. | 若a=b,则CO2与NaOH溶液反应的产物中盐只有Na2CO3 | |
| C. | b可能等于a、小于a或大于a | |
| D. | 不能确定NaOH溶液的物质的量浓度 |
分析 根据Na2CO3+CaCl2═CaCO3↓+2NaCl,NaHCO3与CaCl2不反应,但碳酸钠、碳酸氢钠都与石灰水反应生成碳酸钙沉淀,已知NaOH完全反应,则一定体积的CO2通入V L NaOH溶液中产物不确定,以此来解答.
解答 解:根据Na2CO3+CaCl2═CaCO3↓+2NaCl,NaHCO3与CaCl2不反应,但碳酸钠、碳酸氢钠都与石灰水反应生成碳酸钙沉淀,已知NaOH完全反应,则一定体积的CO2通入V L NaOH溶液中产物为碳酸钠或碳酸钠和碳酸氢钠;
A.因a、b的关系不确定,无法计算参加反应的CO2的体积,故A错误;
B.由A选项可知若a=b,则CO2与NaOH溶液反应生成的盐只有Na2CO3,故B正确;
C.若产物为碳酸钠,碳酸钠与石灰水、CaCl2溶液都能反应生成碳酸钙,则a=b;若产物为碳酸钠和碳酸氢钠,碳酸氢钠与CaCl2溶液不反应,碳酸钠与CaCl2溶液反应生成碳酸钙,但碳酸钠、碳酸氢钠都与石灰水反应生成碳酸钙沉淀,则a>b,但不可能a<b,故C错误;
D.若a、b相等时,由Na2CO3+CaCl2═CaCO3↓+2NaCl~2NaOH可计算NaOH的物质的量,溶液的体积已知,则可以计算浓度,故D错误;
故选:B.
点评 本题考查学生利用化学反应方程式的计算,明确发生的化学反应并准确判断a、b的关系是解答本题的关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol I2(g)与1mol H2(g)充分反应放热Q1 kJ | |
| B. | 1mol气态碘与1mol固态碘所含的能量相差(Q1+Q2)kJ | |
| C. | 反应①的生成物总能量比反应②的生成物总能量高 | |
| D. | 稳定性:I2(g)>I2(s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离苯和硝基苯:蒸馏 | B. | 分离氯化钠与氯化铵固体:升华 | ||
| C. | 分离水和溴乙烷:分液 | D. | 分离氯化钠和硝酸钾:结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物的总键能低于生成物的总键能 | |
| B. | 1mol I2(g)中通入1mol H2(g),反应放热11kJ | |
| C. | 等物质的量时,I2(g)具有的能量低于I2(l) | |
| D. | 平衡时分离出HI(g),正反应速率先减小后增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | B. | HF的电子式: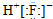 | ||
| C. | S2-的结构示意图: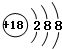 | D. | CCl4分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCl2作为反应物,转移电子数一定为2NA | |
| B. | 1molC9H20中含有共价键数目为28NA | |
| C. | 标况下448mL二氯甲烷中含有分子数为0.02NA | |
| D. | 常温常压下,1.8 g重水(D2O)中含中子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验编号 | HA | NaOH | 混合溶液的pH |
| 甲组 | c(HA)=0.2mol/L | c(NaOH)=0.2mol/L | pH=a |
| 乙组 | c(HA)=0.1mol/L | c(NaOH)=0.1mol/L | pH=9 |
| 丙组 | pH=2 | pH=12 | pH=b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表里属于过渡元素的化合物 | |
| B. | 位于元素周期表里第ⅡA族元素的化合物 | |
| C. | 位于元素周期表里第ⅢA族元素的化合物 | |
| D. | 位于元素周期表里第ⅣA族元素的化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com