
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如下表,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。
A | ||
E |
(1)C在元素周期表中的位置为_______,其简单离子的结构示意图为____。
(2)AE2的化学式为_______。
(3)C、E、F的单质沸点最低的是__________(填化学式)。
(4)C、D、E、F的离子半径由大到小的顺序是___________________(填离子符号)。
(5)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为________________________。
【答案】第二周期第ⅥA族![]() CS2O2S2—>Cl—>O2—>Al3+2NH3H2O+3H2O2=N2↑+8H2O
CS2O2S2—>Cl—>O2—>Al3+2NH3H2O+3H2O2=N2↑+8H2O
【解析】
A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A与氧元素能形成两种无色气体CO和CO2,则A为C元素;结合A、E在元素周期表中的相对位置可知E为S元素;C是地壳中含量最多的元素,则C为O元素;B的原子序数介于A、C之间,则B为N元素;D是地壳中含量最多的金属元素,则D为Al元素,F的原子序数依次最大,则F为Cl元素。
(1)C为O元素,在元素周期表中的位置为第二周期第ⅥA族,其离子的结构示意图为![]() 。(2)A为C元素,E为S元素,则AE2的化学式为CS2。(3)C为O元素,单质为氧气;E为S元素,单质为硫固体;F为Cl元素,单质为氯气,氯气的相对分子质量大于氧气,所以沸点最低的是氧气。(4)C、D、E、F的离子符号以此为O2—、Al3+、S2—、Cl—,离子半径的大小规律是电子层数越多,离子半径越大;具有相同电子层结构的离子,原子序数越大,离子半径越小,则C、D、E、F的离子半径由大到小的顺序是S2—>Cl—>O2—>Al3+。(5)B为N元素,N元素的氢化物为氨气,NH3的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,反应生成氮气与水,反应的化学方程式为:2NH3H2O+3H2O2=N2↑+8H2O。
。(2)A为C元素,E为S元素,则AE2的化学式为CS2。(3)C为O元素,单质为氧气;E为S元素,单质为硫固体;F为Cl元素,单质为氯气,氯气的相对分子质量大于氧气,所以沸点最低的是氧气。(4)C、D、E、F的离子符号以此为O2—、Al3+、S2—、Cl—,离子半径的大小规律是电子层数越多,离子半径越大;具有相同电子层结构的离子,原子序数越大,离子半径越小,则C、D、E、F的离子半径由大到小的顺序是S2—>Cl—>O2—>Al3+。(5)B为N元素,N元素的氢化物为氨气,NH3的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,反应生成氮气与水,反应的化学方程式为:2NH3H2O+3H2O2=N2↑+8H2O。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:
【题目】将Na2O2投入FeCl3溶液中,对观察到的现象描述准确的是 ( )
A.生成白色沉淀
B.既有气泡产生,又生成红褐色沉淀
C.既有气泡产生,又生成白色沉淀
D.有气泡产生,无沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列三个反应:
①Cl2+FeI2=FeCl2+I2
②2Fe2++Br2=2Fe3++2Br-
③Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列说法正确的是( )
A. 反应①②③中的氧化产物分别是I2、Fe3+、CoCl2
B. 根据以上方程式可以得到氧化性:Cl2>Fe3+>Co2O3
C. 在反应③中当1 mol Co2O3参加反应时,2 mol HCl被氧化
D. 可以推理得到Cl2+FeBr2 =FeCl2+Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃分子中有40个电子,它燃烧时生成等体积的CO2和H2O(g),该有机物的分子式为 ( )
A.C4H8
B.C4H10
C.C5H10
D.C5H12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在给定条件下能实现转化的是
①Si![]() Na2SiO3(aq)
Na2SiO3(aq)![]() H2SiO3
H2SiO3
②Na![]() Na2O2
Na2O2![]() NaOH
NaOH
③CaCO3![]() CaO
CaO![]() CaC2
CaC2![]() C2H4
C2H4
④饱和NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
⑤MgCl2(aq)![]() MgCl2·6H2O
MgCl2·6H2O![]() Mg
Mg
⑥CuSO4(aq)![]() Cu(OH)2
Cu(OH)2![]() Cu2O
Cu2O
A. ①④⑥ B. ③④⑤
C. ②⑤⑥ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
A. 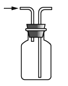 收集 NOB.
收集 NOB.  制备 NH3
制备 NH3
C.  制备 Fe(OH)2D.
制备 Fe(OH)2D. 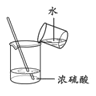 稀释浓 H2SO4
稀释浓 H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸或硝酸在下列用途或反应中各表现的性质是:
A.强酸性 B.易挥发性 C.吸水性 D.脱水性 E.强氧化性 F.不稳定性
(1)胆矾中加入浓硫酸,久置变为白色粉末__________;
(2)用铝槽车装运浓硫酸或浓硝酸___________;
(3)浓硝酸敞口放置会“发烟”___________,
(4)浓硝酸久置会变黄____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)
根据图示回答下列问题:
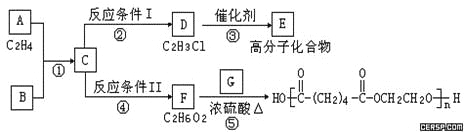
(1)写出A、E、G的结构简式:A ,E ,G ;
(2)反应②的化学方程式(包括反应条件)是 ,反应④化学方程式(包括反应条件)是 ;
(3)写出①、⑤的反应类型:① 、⑤ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来AIST报告正在研制一种“高容量、低成本”锂-铜空气燃料电池。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )

A. 放电时,Li+透过固体电解质向Cu极移动
B. 放电时,负极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH-
C. 通空气时,铜被腐蚀,表面产生Cu2O
D. 整个反应过程中,铜相当于催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com