
(B)����ѧ���л���ѧ��������13�֣�
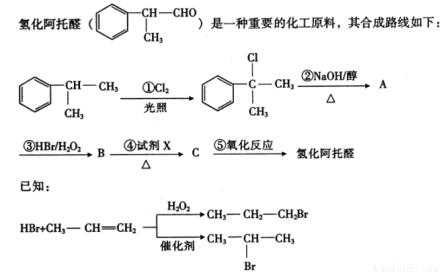
����������ϳ�·�ߣ��ش��������⣺
��1���⻯����ȩ���������ŵ�����Ϊ ��һ�������£�1 mol�⻯����ȩ���ɸ� mol�����ӳɡ�
��2���ڵķ�Ӧ������ ��
��3��д����Ӧ�۵Ļ�ѧ����ʽ�� ��
��4�����������Լ�XΪ ��
��5��C������M��һ�������¿�����һ����Է�������Ϊ178���������ʣ���M�Ľṹ��ʽΪ ��
��6���⻯����ȩ���ж���ͬ���칹�壬д����������������ͬ���칹��Ľṹ��ʽ�� ��д��һ�ּ��ɣ���
�ٱ�����������ȡ����
�ڱ����ϵ�һ�����ֻ������
����ˮ��Һ��FeCl3��Һ��������ɫ
���ܷ����Ӿ۷�Ӧ
��1��ȩ����4 ��2����ȥ��Ӧ ��3��
��4��NaOH��Һ ��5��CH3COOH ��6�� ��
�� ��
��
��������
�����������1�������⻯����ȩ�Ľṹ��ʽ��֪���������ŵ�����Ϊȩ�������ڱ�����ȩ�����������������ӳɷ�Ӧ����һ�������£�1 mol�⻯����ȩ���ɸ�4 mol�����ӳɡ�
��2�����ݷ�Ӧ�ڵ��������������ƵĴ���Һ���жϣ��䷴Ӧ����������ԭ�ӵ���ȥ��Ӧ��
��3��A�к���̼̼˫����������֪��Ϣ��֪��A��˫��ˮ�����������廯�ⷢ���ӳɷ�Ӧ����B����Ӧ�۵Ļ�ѧ����ʽΪ ��
��
��4��C�����õ��⻯����ȩ����˵��C�к����ǻ�����B����C��±������ˮ�ⷴӦ������������Լ�XΪNaOH��Һ��
��5��C�Ľṹ��ʽΪ ��������M��һ�������¿�����һ����Է�������Ϊ178���������ʣ�����������غ㶨�ɿ�֪M����Է���������178+18-136��60������M�����ᣬ���M�Ľṹ��ʽΪCH3COOH��
��������M��һ�������¿�����һ����Է�������Ϊ178���������ʣ�����������غ㶨�ɿ�֪M����Է���������178+18-136��60������M�����ᣬ���M�Ľṹ��ʽΪCH3COOH��
��6���ٱ�����������ȡ�������ڱ����ϵ�һ�����ֻ�����֣�˵������ȡ�����Ƕ�λ�ģ�����ˮ��Һ��FeCl3��Һ��������ɫ��˵�����з��ǻ������ܷ����Ӿ۷�Ӧ��˵��������̼̼˫����������������л���ṹ��ʽΪ ��
�� ��
�� ��
��
���㣺�����л����ƶϡ���Ӧ���͡������š���Ӧ������ͬ���칹���ж��Լ�����ʽ��д��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ������һ�����У�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��6�֣��״�(CH3OH)�Ͷ����ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϡ���CH4��H2OΪԭ���Ʊ��״��Ͷ����ѵĹ�ҵ�������£�
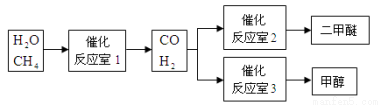
����Ҫ��ش��������⣺
��1������Ӧ��1����һ�������·�Ӧ�Ļ�ѧ����ʽΪ ��
��2��ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2(g)+CO(g) CH3OH(g) ��H = -90.8kJ��mol-1
CH3OH(g) ��H = -90.8kJ��mol-1
��2CH3OH(g) CH3OCH3(g)+H2O(g) ��H = -23.5kJ��mol-1
CH3OCH3(g)+H2O(g) ��H = -23.5kJ��mol-1
��CO(g)+H2O(g) CO2(g)+H2(g) ��H = -41.3kJ��mol-1
CO2(g)+H2(g) ��H = -41.3kJ��mol-1
����Ȼ�ѧ��Ӧ����ʽ��3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)����H = ��
CH3OCH3(g)+CO2(g)����H = ��
��3��ij���л������Ƶ�һ�����͵����ӽ���Ĥ������ȼ�ϵ��(DDFC)���õ���нϸߵİ�ȫ�ԡ��õ���ܷ�ӦΪCH3OCH3+3O2=2CO2+3H2O���乤��ԭ����ͼ��ʾ��
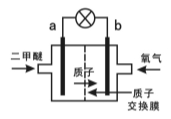
�缫a�ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�Ϫ�ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��12�֣�Ҫ��ȥ�±������л����е����ʣ�������Ϊ���ʣ����ӣ�����ѡ�����˵��Լ����ӣ�����ѡ������ᴿ�ķ����������������С�
��1���Լ���a��Ũ���� b������������Һ c����ʯ�� d��̼������Һ e��ˮ f��Ũ��ˮ
��2��������A������ B����Һ C������
Ҫ�ᴿ������ �����ʣ� | �����飨�Ҵ��� | �Ҵ���ˮ�� | �Ҵ������ᣩ | �屽���壩 | �������ӣ� |
��1��ѡ���Լ� | |||||
��2�����뷽�� |
��3�����ϲ��õIJ����У�Bʹ�õ���Ҫ����������____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�Ϫ�ظ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A�����͡����ͺ�ֲ���Ͷ���̼�⻯����
B��ʯ�͵ķ����ú�ĸ����������仯
C����ά�ء����ۡ���������һ�������¶��ܷ���ˮ�ⷴӦ
D�������ں���̼̼������̼̼˫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ˮ�и�����ѧ��һģ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ݱ��������Ħ��������˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ������ɴ�����ʹ�õ������ػ�﮵�ص�ʮ����������ʹ��һ���²ų�һ�ε硣���ط�ӦΪ��2CH3OH + 3O2 + 4OH�� 2CO32�� + 6H2O��������˵������ȷ����
2CO32�� + 6H2O��������˵������ȷ����
A���ŵ�ʱCH3OH���뷴Ӧ�ĵ缫Ϊ����
B�����ʱ�������Һ��pH������
C���ŵ�ʱ�����ĵ缫��ӦΪ��CH3OH��6e��+8OH����CO32�� +6H2O
D�����ʱÿ����1 mol CH3OHת��6 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и���3��������黯ѧ�Ծ��������棩 ���ͣ������
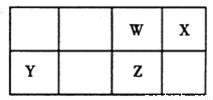
��10�֣�������Ԫ��W��X��Y��Z��Ԫ�����ڱ��е�λ������ͼ��ʾ������Z�ĵ�����һ����Ҫ�뵼����ϣ��㷺Ӧ���ڵ��ӹ�ҵ�ĸ�������
��1��W��Ԫ�����ڱ��е�λ���� ��
��2��Z��ԭ�ӽṹʾ��ͼΪ ��
��3������ѡ���У���֤��Ԫ�طǽ�����Xǿ��W���� ��
A��ԭ��������X>W
B����ͻ��ϼۣ�X>W
C������⻯����ȶ��ԣ�X>W
D������������ˮ�������ԣ�X>W
��4��Ԫ�����ڱ�����Zͬ���ڵ�ij����Ԫ���γɵĵ���A���ɷ�������ͼ��ʾ��ת����
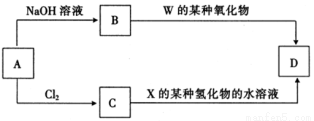
���л�����D��һ�ְ�ɫ��������B�����ʵĻ�ѧʽΪ ��Cת������D�����ӷ���ʽΪ ��
��5������Y������������Ӧˮ����Ļ�ѧʽΪY(OH)n ����T��ʱ���䱥����Һ��ʹ��̪��Һ��죬ԭ��������Һ�е�c(OH��) = mol��L��1 ���������ֵ����֪��T�棬Ksp[Y(OH) n]=4.0��l0-12����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и���3��������黯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£����и��������ܳ����������
A��Mg2+��K+��SO42����NO3�� B��Fe2+��H+��Cl����NO3��
C��Cu2+��Na+��OH����Cl�� D��K+��HCO3����Ca2+��OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�ӱ�ʡ��̨�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͬ�¶�ʱ��100 mL 0.01 mol/L�Ĵ�����Һ��10 mL 0.1 mol/L�Ĵ�����Ƚϣ�������ֵ�У�ǰ�ߴ��ں��ߵ���
A��H+�����ʵ���
B������ĵ��볣��
C���к�ʱ����NaOH�����ʵ���
D��������п�۲�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ������ѧ����ĩ����ѧ�Ծ��������棩 ���ͣ������
��16�֣���Դ��ȱ������������ٵ��ش����⣬���û�ѧ��Ӧ��ʵ�ֶ�����ʽ�������ת������ش��������⣺
��1������̬��̬ԭ���γ�1mol��ѧ���ͷŵ���������м��ܡ��ӻ�ѧ���ĽǶȷ�������ѧ��Ӧ�Ĺ��̾��Ǿɼ����Ѻ��¼����γɹ��̡���֪��ӦN2(g)��3H2(g) 2NH3(g) ��H����93 kJ��mol��1���Ը��ݱ������м������ݣ�����a ����ֵΪ kJ��mol��
2NH3(g) ��H����93 kJ��mol��1���Ը��ݱ������м������ݣ�����a ����ֵΪ kJ��mol��
��ѧ�� | H��H | N��H | N��N |
����/kJ��mol��1 | 436 | a | 945 |
��2���״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������֪�ڳ�ѹ�������±仯��
�� 2CH3OH(l)��3O2(g)��2CO2(g)��4H2O(g) ��H ��a kJ��mol
�� H2O(g)��H2O(l) ��H ��b kJ��mol
д��Һ̬�״���ȫȼ�����ɶ�����̼��Һ̬ˮ���Ȼ�ѧ����ʽ�� ��
��3�������ü״�ȼ�շ�Ӧ���һ��ȼ�ϵ�ء�����ͼ1����Pt���缫���ϣ�������������Һ���������Һ���������缫�Ϸֱ����״���������

��д��ȼ�ϵ�������ĵ缫��Ӧʽ ��
�������ø�ȼ�ϵ���ṩ��Դ����ͼ1�ұ��ձ������������������ͭ��������Ӧ�� �����A����B����������������������6.4gʱ��ȼ�ϵ�������������ı�״�������Ϊ L��
��4�����ģ�ҵ�����ӽ���Ĥ�����ռ�ķ�������ô������������ͼ2װ�õ���������Һ����ȡ������������������������أ������ڵ������ӽ���Ĥֻ����������ͨ���������ӽ���Ĥֻ����������ͨ������
�ٸõ��۵�������ӦʽΪ ����λʱ����ͨ�������ӽ���Ĥ����������ͨ�������ӽ���Ĥ���������ı�ֵΪ ��
�ڴӳ���D��������Һ�� ���ѧʽ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com