
【题目】(题文)含碳物质在日常生活与工业生产上有广泛的应用。
(1)一种熔融碳酸盐燃料电池原理示意如图1所示,写出电极A中发生的电极方程式_____;

(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化见图2。在15小时内,CH4的平均生成速率I、Ⅱ和Ⅲ从大到小的顺序为______________(填序号)。

(3)以 TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3。乙酸的生成速率主要取决于温度影响的范围是______________________;
(4)CO和H2在Cu2O/ZnO作催化剂的条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)获得甲醇。向2L的密闭容器中通入1mol CO(g)和2mol H2(g),发生反应合成甲醇,反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图4所示。
CH3OH(g)获得甲醇。向2L的密闭容器中通入1mol CO(g)和2mol H2(g),发生反应合成甲醇,反应过程中,CH3OH的物质的量(n)与时间(t)及温度的关系如图4所示。
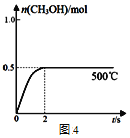
①500℃的此反应的平衡常数K=________________;
②据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量的CO2 有利于维持Cu2O的量不变,原因是________________(用化学方程式表示)。
③在500℃恒压条件下,请在图4中画出反应体系中n(CH3OH)随时间t变化的总趋势图________________。
【答案】H2-2e-+CO32-=CO2+H2O、CO-2e-+CO32-=2CO2Ⅱ>Ⅲ>Ⅰ300℃<T<400℃4Cu2O+CO![]() 2Cu+CO2
2Cu+CO2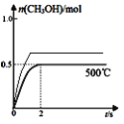
【解析】
(1)燃料电池工作时,通入燃料的为负极,即CO和H2在负极失去电子发生氧化反应,电极反应为:H2-2e-+CO32-=CO2+H2O、CO-2e-+CO32-=2CO2,故答案为:H2-2e-+CO32-=CO2+H2O、CO-2e-+CO32-=2CO2;
(2)由图2可知,在0~15h内,甲烷的物质的量变化量为△n(Ⅰ)<△n(Ⅲ)<△n(Ⅱ),故在0~15h内,CH4的平均生成速率Ⅱ>Ⅲ>Ⅰ,故答案为:Ⅱ>Ⅲ>Ⅰ;
(3)根据图像,温度超过250℃时,催化剂的催化效率降低,在300℃时失去活性,故以后乙酸的生成速率升高是由温度升高导致的,故乙酸主要取决于温度影响的范围为300℃~400℃,故答案为:300℃~400℃;
(4)①根据图像,2s后达到平衡,平衡时甲醇的物质的量为0.5mol,浓度为0.25mol/L,
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始(mol/L) 0.5 1 0
反应(mol/L)0.25 0.5 0.25
平衡(mol/L)0.25 0.5 0.25
500℃的此反应的平衡常数K=![]() =
=![]() =4,故答案为:4;
=4,故答案为:4;
②在加热条件下CO能还原Cu2O使其减少,因此反应体系中含有少量二氧化有利于抑制反应向正反应方向移动,维持Cu2O的量不变,反应方程式为Cu2O+CO2Cu+CO2,故答案为:Cu2O+CO2Cu+CO2;
③合成甲醇:CO(g)+2H2(g)CH3OH(g),反应后气体体积减小,在500℃恒压条件下,容器体积减小压强增大,相当于增大了压强,反应速率加快,达到平衡需要的时间减少,增大压强,平衡正向移动,甲醇的物质的量增大,图像为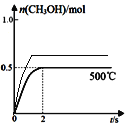 ;故答案为:
;故答案为: ;
;


科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl- 六种粒子。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是
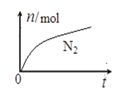
A. 该反应的还原剂是Cl-
B. 消耗1 mol还原剂,转移6 mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为 r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生如图所示变化,其中B和C均为10电子分子。下列说法中正确的是

A. X元素位于第ⅣA族
B. A能溶解于B中
C. A和C不可能发生氧化还原反应
D. B的沸点高于C的沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质组成的说法中,正确的是
A.酸、碱、盐可能都不含金属元素
B.含氧元素的化合物一定是氧化物
C.单质不一定只含一种元素
D.酸、碱中一定含氢,盐一定不含氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气脱硫能有效减少二氧化硫的排放,实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6﹣2x]溶液,并用于烟气脱硫研究。

下列说法错误的是
A. 滤渣Ⅰ的主要成分为SiO2
B. 加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6﹣2x
C. 调节pH时若溶液的pH偏高,将会导致溶液中铝元素的含量降低,相应的离子方程式如下:3CaCO3+2Al3++3H2O=2Al(OH)3+3Ca2++3CO2↑
D. 上述流程中经完全热分解放出的SO2量总是小于吸收的SO2的量,其主要原因是溶液中的部分SO32-被氧化成SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能用胶体的知识解释的现象是
A.豆浆中加入石膏做豆腐
B.一支钢笔使用两种不同牌号的墨水,易出现堵塞
C.向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
D.在海水与河水交界处,易形成三角洲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两份等质量Na2O2和NaHCO3均匀混和物,向其中一份加入100mL盐酸,充分反应呈中性,放出气体经干燥后测得体积为2.24L(标准状况)。如将该气体通入另一混和物中充分反应后,气体体积变为2.016L(标准状况)。若混合物中NaHCO3的物质的量大于Na2O2。则:
(1)原混和物中Na2O2与NaHCO3的物质的量之比为__________________;
(2)加入盐酸的物质的量的浓度为_____________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有 A、B、C、D、E 五种短周期主族元素,原子序数由 A 到 E 逐渐增大.①A 元素最外层电子数是次外层电子数的 2 倍. ②B 的阴离子和 C 的阳离子与氖原子的电子层结构相同.③在通常状况下,B 的单质是气体,0.1molB 的气体与足量的氢气完全反应共有 0.4mol 电子转移.④C 的单质在点燃时与 B 的单质充分反应,生成淡黄色的固体, 此淡黄色固体能与 AB2 反应可生成 B 的单质.⑤D 的气态氢化物与其最高价含氧酸间能发生氧化还原反应.请写出:
(1)A 元素的最高价氧化物的电子式_________________,A 元素简单气态氢化物可构成碱性燃料电池,该电池的的负极电极方程式为:_____________________
(2)B 元素在周期表中的位置 _____________________
(3)B 单质与 C 单质在点燃时反应的生成物中所含化学键类型有 _________________
(4)D 元素的低价氧化物与 E 的单质的水溶液反应的化学方程式为 :____________________
(5)C 与 D 能形成 2:1 的化合物,用电子式表示该化合物的形成过程:_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com