
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
2N2O5 (g)  4NO2(g)+ O2(g) △H >0
4NO2(g)+ O2(g) △H >0
T1温度下的部分实验数据为:
t/s | 0 | 500 | 1000 | 1500 |
c(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法不正确的是
A.500s内N2O5分解速率为2.96×10—3 mol/(L· s)
B.T1温度下的平衡常数为K1 =125(mol/L)3,1000s时转化率为50%
C.T1温度下的平衡常数为K1 ,T3温度下的平衡常数为K3,若T1 >T3,则K1> K3
D.其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,则T1 <T2
科目:高中化学 来源: 题型:
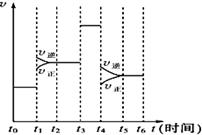
右图表示反应N2(g)+3H2(g) 2NH3(g) △H<0在某一
时间段中反应速率与反应过程的曲线关系。下列说法正确的是
A.氨气的体积分数最高的一段时间为t5-t6
B.t2-t3和t3-t4时间段氨气的体积分数相等
C.t1时刻改变的条件是降低温度
D.t4-t5时间段平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水所含的三种离子是________、_________、_________。
(2)乙厂的废水中含有另外三种离子。如果加一定量________(选填:活性炭、硫酸亚铁、硫酸亚铁、铁粉),可能回收其中的金属__________(填元素符号)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.在实验室里硅酸钠溶液存放在带橡胶塞的试剂瓶中
B.提倡人们购物时不用塑料袋,是为了防止白色污染
C.氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应”
D.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏伽德罗常数的值。下列说正确的是
A.高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO32HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
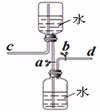
右图是某同学设计的储气装置(固定装置已略去),下列说法中,不正确的是
A.打开止水夹a、b,气体从d管导入,储存在下面的集气瓶里
B.取用储存在下面集气瓶里的气体时,通过控制止水夹a、b,
可将气体顺利排出
C.气体被储存在下面的集气瓶里时,c导管也必须安装止水夹
D.该装置也可作为制取二氧化碳气体的发生装置
查看答案和解析>>
科目:高中化学 来源: 题型:
已知Q与R的摩尔质量之比为9∶22,在反应X+2Y===2Q+R中,当1.6 g X与Y完全反应后,生成4.4 g R,则参与反应的Y和生成物Q的质量之比为( )
A.46∶9 B.32∶9
C.23∶9 D.16∶9
查看答案和解析>>
科目:高中化学 来源: 题型:
用化学术语回答下列问题:
(1)由氢气和氧气反应生成1 mol水蒸气放热241.8 kJ·mol-1,写出其热化学方程式: .
若1g水蒸气转化成液态水放热2.444kJ,则反应H2(g)+1/2 O2(g)==H2O(l)
的△H= kJ·mol-1,氢气的燃烧热为 kJ·mol-1。
(2)电解硝酸银溶液电极反应式(惰性电极)
①阳极:
②阴极:
(3)银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为:
2Ag+Zn(OH)2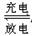 Ag2O+Zn+H2O在此电池放电时,正极的电极反应式为 。
Ag2O+Zn+H2O在此电池放电时,正极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com