
”¾ĢāÄæ”æĻć¶¹ĖŲŹĒŅ»ÖÖÓĆĶ¾¹ć·ŗµÄĻćĮĻ£¬æÉÓĆÓŚÅäÖĘĻć¾«ŅŌ¼°ÖĘŌģČÕÓĆ»ÆױʷŗĶĻćŌķµČ”£ŅŌÓŠ»śĪļMŗĶÓŠ»śĪļAŗĻ³ÉĻć¶¹ĖŲµÄĮ÷³ĢČēĻĀ£ŗ

ŅŃÖŖŅŌĻĀŠÅĻ¢£ŗ
¢Ł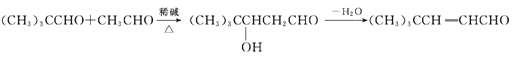
¢Ś MµÄ·Ö×ÓŹ½ĪŖC2H6O£¬·Ö×ÓÖŠÓŠ3ÖÖ»Æѧ»·¾³²»Ķ¬µÄĒāŌ×Ó
¢Ū Ļć¶¹ĖŲÖŠŗ¬ÓŠĮ½øöĮłŌŖ»·
(l) MµÄ»ÆѧĆū³ĘŹĒ______£¬ÓÉMÉś³ÉBµÄ»Æѧ·½³ĢŹ½ĪŖ_______”£
(2) AµÄ½į¹¹¼ņŹ½ĪŖ________”£
(3) D×Ŗ±äĪŖEµÄµŚ¢Ł²½ĖłŠčµÄŹŌ¼Į¼°·“Ó¦Ģõ¼žŹĒ________”£
(4£©ÓÉEÉś³ÉĻć¶¹ĖŲµÄ»Æѧ·½³ĢŹ½ĪŖ________”£
(5£©Š“³öĀś×ćČēĻĀĢõ¼žµÄCµÄŅ»ÖÖĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ________”£
¢Ł ÄÜ·¢ÉśŅų¾µ·“Ó¦ ¢Ś 1mol CĶźČ«·“Ó¦ÄÜĻūŗÄ2 mol NaOH
¢Ū ±½»·ÉĻÓŠ3øöČ”“ś»ł ¢Ü ±½»·ÉĻµÄŅ»ĀČ“śĪļÖ»ÓŠ2ÖÖ
”¾“š°ø”æ ŅŅ“¼ 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O ![]() Ņų°±ČÜŅŗ”¢Ė®Ō”¼ÓČČ£Ø»ņŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ”¢¼ÓČČ”¢²»ÄÜÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬Ėü»įŃõ»ÆĖ«¼ü¼°·ÓĢž»ł£»Ņ²²»ÄÜÓĆO2£¬Ėü»įŃõ»Æ·ÓōĒ»ł£©
Ņų°±ČÜŅŗ”¢Ė®Ō”¼ÓČČ£Ø»ņŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ”¢¼ÓČČ”¢²»ÄÜÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬Ėü»įŃõ»ÆĖ«¼ü¼°·ÓĢž»ł£»Ņ²²»ÄÜÓĆO2£¬Ėü»įŃõ»Æ·ÓōĒ»ł£© 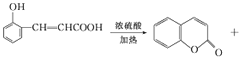 H2O
H2O 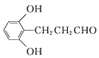 £¬
£¬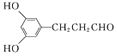 £¬
£¬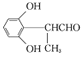 £¬
£¬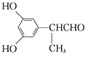 £ØČĪŠ“Ņ»ÖÖ£©
£ØČĪŠ“Ņ»ÖÖ£©
”¾½āĪö”æøł¾ŻĮ÷³ĢŅŌ¼°ŅŃÖŖ¢Ł¢ŚæÉÖŖA”¢B¶¼ŗ¬ÓŠČ©»ł£¬ŌņMĪŖŅŅ“¼£¬BĪŖŅŅČ©£¬AĪŖ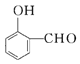 £¬øł¾ŻŅŃÖŖ¢Ū Ļć¶¹ĖŲÖŠŗ¬ÓŠĮ½øöĮłŌŖ»·£¬ŌņÓ¦ĪŖEĶعż·Ö×ÓÄŚõ„»Æ¶ųµĆ£¬¹ŹĻć¶¹ĖŲĪŖ£ŗ
£¬øł¾ŻŅŃÖŖ¢Ū Ļć¶¹ĖŲÖŠŗ¬ÓŠĮ½øöĮłŌŖ»·£¬ŌņÓ¦ĪŖEĶعż·Ö×ÓÄŚõ„»Æ¶ųµĆ£¬¹ŹĻć¶¹ĖŲĪŖ£ŗ![]() ”£(l) MµÄ»ÆѧĆū³ĘŹĒŅŅ“¼£¬ÓÉMÉś³ÉBµÄ»Æѧ·½³ĢŹ½ĪŖ2CH3CH2OH+O2
”£(l) MµÄ»ÆѧĆū³ĘŹĒŅŅ“¼£¬ÓÉMÉś³ÉBµÄ»Æѧ·½³ĢŹ½ĪŖ2CH3CH2OH+O2![]() 2CH3CHO+2H2O£»(2) AµÄ½į¹¹¼ņŹ½ĪŖ
2CH3CHO+2H2O£»(2) AµÄ½į¹¹¼ņŹ½ĪŖ £»(3) D×Ŗ±äĪŖEµÄµŚ¢Ł²½ŹĒČ©Ńõ»ÆÉś³ÉōČĖį£¬ĖłŠčµÄŹŌ¼Į¼°·“Ó¦Ģõ¼žŹĒŅų°±ČÜŅŗ”¢Ė®Ō”¼ÓČČ£Ø»ņŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ”¢¼ÓČČ”¢²»ÄÜÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬Ėü»įŃõ»ÆĖ«¼ü¼°·ÓĢž»ł£»Ņ²²»ÄÜÓĆO2£¬Ėü»įŃõ»Æ·ÓōĒ»ł£©£»(4£©ÓÉE·¢Éś·Ö×ÓÄŚõ„»ÆÉś³ÉĻć¶¹ĖŲµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
£»(3) D×Ŗ±äĪŖEµÄµŚ¢Ł²½ŹĒČ©Ńõ»ÆÉś³ÉōČĖį£¬ĖłŠčµÄŹŌ¼Į¼°·“Ó¦Ģõ¼žŹĒŅų°±ČÜŅŗ”¢Ė®Ō”¼ÓČČ£Ø»ņŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ”¢¼ÓČČ”¢²»ÄÜÓĆĖįŠŌøßĆĢĖį¼ŲČÜŅŗ£¬Ėü»įŃõ»ÆĖ«¼ü¼°·ÓĢž»ł£»Ņ²²»ÄÜÓĆO2£¬Ėü»įŃõ»Æ·ÓōĒ»ł£©£»(4£©ÓÉE·¢Éś·Ö×ÓÄŚõ„»ÆÉś³ÉĻć¶¹ĖŲµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ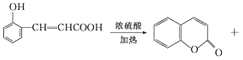 H2O£»(5£©CµÄĶ¬·ÖŅģ¹¹Ģå£ŗ¢Ł ÄÜ·¢ÉśŅų¾µ·“Ó¦Ö¤Ć÷½į¹¹ÖŠŗ¬ÓŠČ©»ł£¬
H2O£»(5£©CµÄĶ¬·ÖŅģ¹¹Ģå£ŗ¢Ł ÄÜ·¢ÉśŅų¾µ·“Ó¦Ö¤Ć÷½į¹¹ÖŠŗ¬ÓŠČ©»ł£¬
¢Ū ±½»·ÉĻÓŠ3øöČ”“ś»łĒŅ ±½»·ÉĻµÄŅ»ĀČ“śĪļÖ»ÓŠ2ÖÖ£¬·Ö×Óø߶ȶŌ³ĘĒŅÓ¦øĆÓŠĮ½øöČ”“ś»łŹĒŅ»ŃłµÄ£¬¢Ś 1mol CĶźČ«·“Ó¦ÄÜĻūŗÄ2 mol NaOH£¬Č©»ł²»ÓėĒāŃõ»ÆÄĘ·“Ó¦£¬¹ŹĮķĶāµÄČ”“ś»łÓ¦øĆŹĒ·ÓōĒ»łĮ½øö£¬·ūŗĻĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ£ŗ £¬
£¬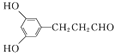 £¬
£¬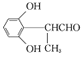 £¬
£¬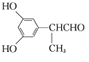 ”£
ӣ



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·ŹĒ£Ø””””£©
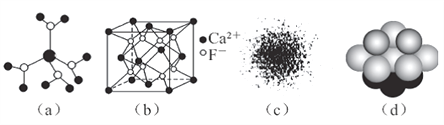
A. Ė®ŗĻĶĄė×ÓµÄÄ£ŠĶČēĶ¼(a)ĖłŹ¾£¬1øöĖ®ŗĻĶĄė×ÓÖŠÓŠ4øöÅäĪ»Ģå
B. CaF2¾§ĢåµÄ¾§°ūČēĶ¼(b)ĖłŹ¾£¬ĆæøöCaF2¾§°ūĘ½¾łÕ¼ÓŠ4øöCa2£«
C. HŌ×ӵĵē×ÓŌĘĶ¼ČēĶ¼(c)ĖłŹ¾£¬HŌ×ÓŗĖĶā“󶹏żµē×ÓŌŚŌ×ÓŗĖø½½üŌĖ¶Æ
D. ½šŹōCuÖŠCuŌ×ӶѻżÄ£ŠĶČēĶ¼(d)£¬ĪŖ×īĆܶѻż£¬ĆæøöCuŌ×ÓµÄÅäĪ»Źż¾łĪŖ12
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēŗĪ·ĄÖ¹ĢśµÄŠāŹ“ŹĒ¹¤ŅµÉĻŃŠ¾æµÄÖŲµćÄŚČŻ”£ĪŖŃŠ¾æĢśµÄŠāŹ“,ijĶ¬Ń§×öĮĖĢ½¾æŹµŃé,ČēĻĀĶ¼ĖłŹ¾,Ģś“¦ÓŚ¢Ł¢Ś¢ŪČżÖÖ²»Ķ¬µÄ»·¾³ÖŠ

Ēė»Ų“š:
£Ø1£©½šŹōøÆŹ“Ö÷ŅŖ·ÖĪŖ__________øÆŹ“ŗĶ_____________øÆŹ“Į½ÖÖ”£
£Ø2£©Ģś±»øÆŹ“µÄĖŁĀŹÓÉæģµ½ĀżµÄĖ³ŠņŹĒ_________________(ĢīŠņŗÅ)”£
£Ø3£©¢ŁÖŠÕż¼«µÄµē¼«·“Ó¦Ź½ĪŖ_________________________________________________£¬¢ŚÖŠøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_________________________________________”£
£Ø4£©¾Ż×ŹĮĻĻŌŹ¾,Č«ŹĄ½ēĆæÄźŅņøÆŹ“¶ų±Ø·ĻµÄ½šŹō²ÄĮĻĻąµ±ÓŚĘäÄź²śĮæµÄ20%ŅŌÉĻ”£ĪŖ·Ą»¤½šŹō±»øÆŹ“æɲÉČ”µÄ“ėŹ©ÓŠ__________(ĢīŠņŗÅ)”£
¢Ł½”ÉķĘ÷²ÄĖ¢ÓĶĘį ¢Ś×ŌŠŠ³µøÖȦ¶Ęøõ
¢Ū½«øÖ¹ÜÓƵ¼ĻßÓėĶĢõĮ¬½Ó ¢Ü½«øÖ¹ÜÓƵ¼ĻßÓėĢ¼°ōĮ¬½Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚĀČĖ®µÄŠšŹö²»ÕżČ·µÄŹĒ
A. ŠĀÖĘĀČĖ®ÖŠÖ»ŗ¬Cl2ŗĶH2OĮ½ÖÖ·Ö×Ó
B. ŠĀÖĘĀČĖ®æÉŹ¹Ą¶É«ŹÆČļŹŌÖ½ĻȱäŗģŗóĶŹÉ«
C. ¹āÕÕĀČĖ®ÓŠĘųÅŻ²śÉś£¬øĆĘųĢåŹĒO2
D. ĀČĖ®³¤Ź±¼ä·ÅÖĆŗóĖįŠŌŌöĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°¢ĪŗĖį»ÆѧĆū³ĘĪŖ4ōĒ»ł3¼×Ńõ»łČā¹šĖį£¬æÉŅŌ×öŅ½Ņ©”¢±£½”Ę·”¢»ÆױʷŌĮĻŗĶŹ³Ę·Ģķ¼Ó¼Į£¬½į¹¹¼ņŹ½ĪŖ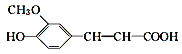 ”£ŌŚ°¢ĪŗĖįČÜŅŗÖŠ¼ÓČėŗĻŹŹŹŌ¼Į(æÉŅŌ¼ÓČČ)£¬¼ģŃéĘä¹ŁÄÜĶÅ”£ĻĀĮŠŹŌ¼Į”¢ĻÖĻ󔢽įĀŪ¶¼ÕżČ·µÄŹĒ£Ø £©
”£ŌŚ°¢ĪŗĖįČÜŅŗÖŠ¼ÓČėŗĻŹŹŹŌ¼Į(æÉŅŌ¼ÓČČ)£¬¼ģŃéĘä¹ŁÄÜĶÅ”£ĻĀĮŠŹŌ¼Į”¢ĻÖĻ󔢽įĀŪ¶¼ÕżČ·µÄŹĒ£Ø £©
Ń”Ļī | ŹŌ¼Į | ĻÖĻó | ½įĀŪ |
A | ĀČ»ÆĢśČÜŅŗ | ČÜŅŗ±äĄ¶É« | Ėüŗ¬ÓŠ·ÓōĒ»ł |
B | Ņų°±ČÜŅŗ | ²śÉśŅų¾µ | Ėüŗ¬ÓŠČ©»ł |
C | Ģ¼ĖįĒāÄĘČÜŅŗ | ²śÉśĘųÅŻ | Ėüŗ¬ÓŠōČ»ł |
D | äåĖ® | ČÜŅŗĶŹÉ« | Ėüŗ¬ÓŠĢ¼Ģ¼Ė«¼ü |
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧæĪĶāŠ”×éÉč¼ĘĮĖČēĶ¼ĖłŹ¾µÄ×°ÖĆÖĘČ”ŅŅĖįŅŅõ„£ØĶ¼ÖŠ¼Š³ÖŅĒĘ÷ŗĶ¼ÓČČ×°ÖĆŅŃĀŌČ„£©£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ

(1)Ė®“ÓĄäÄż¹ÜµÄ______£ØĢī”°a”±»ņ”°b”±£©“¦½ųČė”£
(2)ŅŃÖŖĻĀĮŠŹż¾Ż£ŗ
ŅŅ“¼ | ŅŅĖį | ŅŅĖįŅŅõ„ | 98%ÅØĮņĖį | |
ČŪµć/”ę | ©117.3 | 16.6 | ©83.6 | © |
·Šµć/”ę | 78.5 | 117.9 | 77.5 | 338.0 |
ÓÖÖŖĪĀ¶ČøßÓŚ140”ꏱ·¢Éśø±·“Ó¦£ŗ2CH3CH2OH”śCH3CH2OCH2CH3+H2O
¢ŁøĆø±·“Ó¦ŹōÓŚ__________·“Ó¦£ØĢī×ÖÄø£©”£
a£®¼Ó³É b£®Č”“ś c£®õ„»Æ
¢Śæ¼ĀĒµ½·“Ó¦ĖŁĀŹµČ¶ąÖÖŅņĖŲ£¬ÓĆÉĻŹö×°ÖĆÖʱøŅŅĖįŅŅõ„Ź±£¬·“Ó¦µÄ×ī¼ŃĪĀ¶Č·¶Ī§ŹĒ______£ØĢī×ÖÄø£©”£
a£®T£¼77.5”ę b£®T£¾150”ę c£®115”ę£¼T£¼130”ę
(3)ÉĻŹöŹµŃéÖŠ±„ŗĶĢ¼ĖįÄĘČÜŅŗµÄ×÷ÓĆŹĒ£ØĢī×ÖÄø£©£ŗ___________”£
A£®ÖŠŗĶŅŅĖįŗĶŅŅ“¼
B£®ÖŠŗĶŅŅĖį²¢ĪüŹÕ²æ·ÖŅŅ“¼
C£®ŅŅĖįŅŅõ„ŌŚ±„ŗĶĢ¼ĖįÄĘČÜŅŗÖŠµÄČܽā¶Č±ČŌŚĖ®ÖŠøüŠ”£¬ÓŠĄūÓŚ·Ö²ćĪö³ö
D£®¼ÓĖŁõ„µÄÉś³É£¬ĢįøßĘä²śĀŹ
(4)Óū·ÖĄė³öŅŅĖįŅŅõ„£¬Ó¦Ź¹ÓƵķ֥ė·½·ØŹĒ__________£ØĢī²Ł×÷·½·ØĆū³Ę£¬ĻĀĶ¬£©£¬ĖłÓƵ½µÄŅĒĘ÷ĪŖ______ £¬ ½ųŠŠ“Ė²½²Ł×÷ŗó£¬ĖłµĆÓŠ»ś²ćÖŠµÄÖ÷ŅŖĪŽ»śĪļŌÓÖŹŹĒĖ®£¬ŌŚ²»ŌŹŠķŹ¹ÓĆøÉŌļ¼ĮµÄĢõ¼žĻĀ£¬³żČ„Ė®æÉÓĆ____________µÄ·½·Ø”£
(5)ČōŹµŃéĖłÓĆŅŅĖįÖŹĮæĪŖ6.0g£¬ŅŅ“¼ÖŹĮæĪŖ5.0g£¬µĆµ½“æ¾»µÄ²śĘ·ÖŹĮæĪŖ4.4g£¬ŌņŅŅĖįŅŅõ„µÄ²śĀŹŹĒ_______”£
(6)ŅŅ¶žĖįŗĶŅŅ¶ž“¼Ņ²ÄÜ·¢Éśõ„»Æ·“Ó¦£¬Š“³öÉś³É»·õ„µÄ»Æѧ·“Ó¦·½³ĢŹ½____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÅŠ¶ĻĻĀĮŠŌŖĖŲÖŠ²»ŹōÓŚÖ÷×åŌŖĖŲµÄŹĒ£Ø £©
A.Ģś
B.ÄĘ
C.Į×
D.ĀČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI£®³£ĪĀĻĀ£¬HNO2µēĄė·“Ó¦µÄĘ½ŗā³£ŹżÖµĪŖ2.6”Į10-4”£NaNO2ŹĒŅ»ÖÖÖŲŅŖµÄŹ³Ę·Ģķ¼Ó¼Į£¬ÓÉÓŚĘäĶā¹Ū¼°Ī¶µĄ¶¼ÓėŹ³ŃĪ·Ē³£ĻąĖĘ£¬ĪóŹ³¹¤ŅµÓĆŃĪŌģ³ÉŹ³ĪļÖŠ¶¾µÄŹĀ¼žŹ±ÓŠ·¢Éś”£
£Ø1£©Ä³»ī¶ÆŠ”×éĶ¬Ń§Éč¼ĘŹµŃé·½°ø¼ų±š NaClČÜŅŗŗĶNaNO2ČÜŅŗ£¬ĒėĢīŠ“ĻĀĮŠ±ķøń”£
Ń”ÓĆŅ©Ę· | ŹµŃéĻÖĻó | ĄūÓĆNaNO2µÄŠŌÖŹ |
¢Ł·ÓĢŖŹŌŅŗ | ____________ | ____________ |
¢Śµķ·Ū-KIŹŌÖ½ | ____________ | ____________ |
£Ø2£©ŃĒĻõĖįÄĘÓŠ¶¾£¬²»ÄÜĖęŅāÅÅ·Å£¬ŹµŃéŹŅŅ»°ć½«ĘäÓė±„ŗĶĀČ»Æļ§ČÜŅŗ¹²ČČŹ¹Ö®×Ŗ»Æ³ÉĪŽ¶¾ĪŽ¹«ŗ¦µÄĪļÖŹ£¬Ęä²śĪļÖ®Ņ»ĪŖĪŽÉ«ĪŽĪ¶ĘųĢ壬ŌņøĆĘųĢåĪŖ____________£ØĢī»ÆѧŹ½£©”£
II£®»ī¶ÆŠ”×éĶ¬Ń§²ÉÓĆČēĻĀ×°ÖĆÖʱø²¢²ā¶ØĖłµĆ¹ĢĢåÖŠŃĒĻõĖįÄĘ£ØNaNO2£©µÄÖŹĮæ·ÖŹż£Ø×°ÖĆæÉÖŲø“Ź¹ÓĆ£¬²æ·Ö¼Š³ÖŅĒĘ÷ŅŃŹ”ĀŌ£©”£
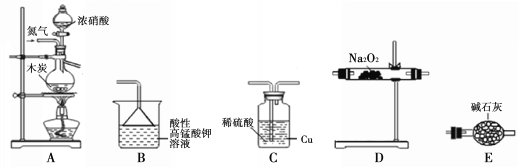
ŅŃÖŖ£ŗ ¢Ł2NO + Na2O2 £½2NaNO2£»
¢ŚĖįŠŌĢõ¼žĻĀ£¬NO”¢NO2¶¼ÄÜÓėMnO4£·“Ӧɜ³ÉNO3£ŗĶMn2+£»NaNO2ÄÜŹ¹
ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«”£
£Ø1£©ŹµŃé×°ÖƵÄĮ¬½ÓĖ³ŠņĪŖ____________£»
£Ø2£©CĘæÄŚ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________”£
£Ø3£©ĪŖĮĖ²ā¶ØŃĒĻõĖįÄʵÄŗ¬Į棬³ĘČ”4.0gѳʷČÜÓŚĖ®Åä³É250mLČÜŅŗ£¬Č”25.00mLČÜŅŗӌ׶ŠĪĘæÖŠ£¬ÓĆ0.10 mol”¤L£1µÄĖįŠŌKMnO4ČÜŅŗ½ųŠŠµĪ¶Ø£¬ŹµŃéĖłµĆŹż¾ŻČēĻĀ±ķ”£
µĪ¶Ø“ĪŹż | 1 | 2 | 3 | 4 |
KMnO4ČÜŅŗĢå»ż/mL | 20.60 | 20.02 | 20.00 | 19.98 |
¢ŁµŚŅ»×鏵Ń鏿¾Ż³öĻÖ½ĻĆ÷ĻŌŅģ³££¬Ōģ³ÉŅģ³£µÄŌŅņæÉÄÜŹĒ__________£ØĢī×ÖÄøŠņŗÅ£©”£
a£®ĖįŹ½µĪ¶Ø¹ÜÓĆÕōĮóĖ®Ļ“¾»ŗóĪ“ÓƱź×¼ŅŗČóĻ“
b£®×¶ŠĪĘæÓĆÕōĮóĖ®Ļ“¾»ŗóĪ“øÉŌļ
c£®¹Ū²ģµĪ¶ØÖÕµćŹ±ŃöŹÓ¶ĮŹż
¢Śøł¾Ż±ķÖŠŹż¾Ż½ųŠŠ¼ĘĖć£¬ĖłÖĘµĆµÄ¹ĢĢåÖŠŃĒĻõĖįÄʵÄÖŹĮæ·ÖŹżĪŖ____________”£
£Ø4£©Éč¼ĘŹµŃ飬±Č½Ļ0.1mol”¤L£1NaNO2ČÜŅŗÖŠNO2£µÄĖ®½ā³Ģ¶ČŗĶ0.1mol”¤L£1HNO2ČÜŅŗÖŠHNO2µēĄė³Ģ¶ČµÄĻą¶Ō“óŠ”_______£Ø¼ņŅŖĖµĆ÷ŹµŃé²½Öč”¢ĻÖĻóŗĶ½įĀŪ£¬ŅĒĘ÷ŗĶŅ©Ę·×ŌŃ”£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫2.3g½šŹōNaĶ¶ČėŅ»¶ØÖŹĮæµÄĖ®ÖŠ£¬»į·¢Éś¾ēĮŅ·“Ó¦£ŗ2Na£«2H2O===2NaOH£«H2”ü,
£Ø1£©·“Ó¦²śÉś±źæöĻĀH2Ģå»żĪŖ¶ąÉŁ£æ_________
£Ø2£©ŅŖŹ¹Ćæ10øöH2OÖŠŗ¬Ņ»øöNa£«£¬ĖłŠčĖ®µÄÖŹĮæĪŖ¶ąÉŁ£æ_____
£Ø3£©ÉĻŹöĖłµĆČÜŅŗĆܶČĪŖ1.20g/mL£¬ĒóČÜŅŗÖŠNaOHµÄÖŹĮæ·ÖŹżŗĶĪļÖŹµÄĮæÅضČø÷ĪŖ¶ąÉŁ£æ£ØŅŖĒ󊓳ö¼ĘĖć¹ż³Ģ£©__________
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com