
| A. | 用SO2漂白纸浆和草帽辫 | |
| B. | SO2具有强还原性,浓硫酸具有强氧化性,故浓硫酸不能用于干燥SO2气体 | |
| C. | 将浓硫酸滴到蔗糖表面,固体变黑膨胀,说明浓硫酸有脱水性和强氧化性 | |
| D. | Na2SO3与H2O2的反应为氧化还原反应 |
分析 A、二氧化硫具有漂白性,可以漂白有机色素;
B.浓硫酸具有强氧化性,但不能氧化二氧化硫;
C.蔗糖变黑,说明浓硫酸具有脱水性,体积膨胀,说明生成气体,表现了浓硫酸的强氧化性;
D.亚硫酸钠具有还原性,过氧化氢具有氧化性二者能发生氧化还原反应;
解答 解:A、二氧化硫具有漂白性,可以漂白有机色素,用SO2漂白纸浆和草帽辫,故A合理;
B.浓硫酸具有强氧化性,二氧化硫具有还原性,硫元素化合价为+4和+6价,同元素相邻价态步方式氧化还原反应,浓硫酸不能氧化二氧化硫,所以能干燥二氧化硫,故B不合理;
C.蔗糖变黑,说明浓硫酸具有脱水性,体积膨胀,说明生成气体,表现了浓硫酸的强氧化性,故C合理;
D.亚硫酸钠具有还原性,过氧化氢具有氧化性二者能发生氧化还原反应生成硫酸钠和水,故D正确;
故选B.
点评 本题考查了物质性质的理解应用,主要是二氧化硫、浓硫酸、亚硫酸钠等物质性质,注意知识的积累,题目难度中等.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:填空题
 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
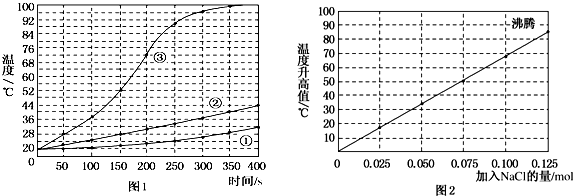
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池可在常温或高温时工作,对环境有较强的适应性 | |
| B. | 负极反应为H2+2OH--2e-=2H2O | |
| C. | 该电池工作时负极有CO2生成 | |
| D. | 该电池供应2molH2O,同时转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:碘化氢>溴化氢>氯化氢 | B. | 氧化性:K+<Na+ | ||
| C. | 最高正化合价:氯>硫>磷 | D. | 原子半径:钠>硫>氯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 变化 | △H | △S | 方向性 | |
| A | H2O(l)→H2O(g) | >0 | <0 | 非自发 |
| B | 2NO2(g)?N2O4(g) | <0 | <0 | 自发 |
| C | 2Fe3+(aq)+Cu(s)=2Fe2+(aq)+Cu2+(aq) | >0 | >0 | 自发 |
| D | NH4Cl(s)=NH3(g)+HCl(g) | <0 | >0 | 非自发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W | |
| T |
 (写电子式);
(写电子式);查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 分子中,一定在同一平面内的碳原子数为a,一定在同一直线上的碳原子数为b,处于四面体结构中心的碳原子数为c.则a,b,c依次为( )
分子中,一定在同一平面内的碳原子数为a,一定在同一直线上的碳原子数为b,处于四面体结构中心的碳原子数为c.则a,b,c依次为( )| A. | 4,5,3 | B. | 4,6,3 | C. | 6,3,4 | D. | 4,4,6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com