
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24L Cl2溶于水或NaOH溶液中转移的电子数均为0.1NA
B. 常温常压下,18g H2O含有的氢原子总数为NA
C. 2.3g钠在足量的氧气中燃烧,转移的电子数为0.1NA
D. 0.1mol CH3OH中所含C-H键的数目为0.4NA
【答案】C
【解析】
A. 标况下,2.24 L氯气的物质的量为0.1 mol,因为氯气和水反应是可逆的,所以无法完全进行,因此转移电子少于0.1 mol,而和氢氧化钠却完全反应,转移0.1 mol电子,A项错误;
B. 18g水的物质的量为:![]() =1 mol,1 mol水分子中含有氢原子的物质的量为2mol,含有的氢原子总数为2NA,B项错误;
=1 mol,1 mol水分子中含有氢原子的物质的量为2mol,含有的氢原子总数为2NA,B项错误;
C. 2.3g钠的物质的量为0.1mol,而钠反应后变为+1价,故0.1 mol钠反应后转移0.1 NA个电子,C项正确;
D. 1mol CH3OH含3mol CH键,故0.1mol CH3OH中所含C-H键的数目为0.3NA,D项错误;
答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(MnS)=2.5×10-13,常温下三种物质在水中的沉淀溶解平衡线如图所示(X表示Fe、Cu、Mn)。下列说法正确的是

A. 曲线Ⅰ表示CuS的溶解平衡曲线
B. MnS在a点溶液中的溶度积等于在b点溶液中的溶度积
C. c点与d点溶液中S2-的物质的量浓度相等
D. 向含有XS固体的d点溶液中滴加稀硫酸至过量可使固体逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】看下列仪器装置图,回答下列问题:
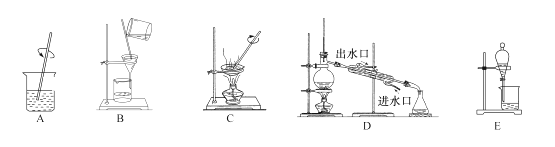
(1)粗盐的提纯需要上面的哪些装置?___________(填字母符号)
(2)分离以下混合物应该选择使用什么装置?(填字母符号)
①酒精和水:___________,
②食盐和水:___________,
③二氧化锰和KCl:___________,
④花生油和水:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PCl3是磷的常见氯化物,可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
熔点/℃ | 沸点/℃ | 密度/ g·mL-1 | 其他 | |
黄磷 | 44.1 | 280.5 | 1.82 | 2P+3Cl2(少量) |
PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
(一)制备
如图是实验室制备PCl3的装置(部分仪器已省略)。

(1)仪器乙的名称是________;其中,与自来水进水管连接的接口编号是________。(填“a”或“b”)
(2)实验室制备Cl2的离子方程式___________________________。实验过程中,为减少PCl5的生成,应控制____________。
(3)碱石灰的作用:一是防止空气中的水蒸气进入而使PCl3水解,影响产品的纯度;二是_________。
(4)向仪器甲中通入干燥Cl2之前,应先通入一段时间CO2排尽装置中的空气,其目的是________。
(二)分析
测定产品中PCl3纯度的方法如下:迅速称取4.100 g产品,水解完全后配成500 mL溶液,取出25.00 mL加入过量的0.100 0 mol·L-1 20.00 mL碘溶液,充分反应后再用0.100 0 mol·L-1 Na2S2O3溶液滴定过量的碘,终点时消耗12.00 mL Na2S2O3溶液。
已知:H3PO3+H2O+I2===H3PO4+2HI;I2+2Na2S2O3===2NaI+Na2S4O6;假设测定过程中没有其他反应。
(5)根据上述数据,该产品中PCl3(相对分子质量为137.5)的质量分数为________。若滴定终点时俯视读数,则PCl3的质量分数________(填“偏大”“偏小”或“无影响”)。
(三)探究
(6)设计实验证明PCl3具有还原性:_____________________________________。(限选试剂有:蒸馏水、稀盐酸、碘水、淀粉)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要用480mL0.1molL-1的硫酸铜溶液,以下配制方法正确的是( )
A. 称取![]() 胆矾(CuSO4·5H2O),配成500mL溶液
胆矾(CuSO4·5H2O),配成500mL溶液
B. 称取![]() 胆矾(CuSO4·5H2O),加入500mL水配成溶液
胆矾(CuSO4·5H2O),加入500mL水配成溶液
C. 称取![]() 无水硫酸铜粉末,加入480mL水配成溶液
无水硫酸铜粉末,加入480mL水配成溶液
D. 称取![]() 无水硫酸铜粉末,加入500mL水配成溶液
无水硫酸铜粉末,加入500mL水配成溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术发展史上的一项重大突破,2018年是合成氨工业先驱哈伯(P·Haber)获得诺贝尔奖100周年
(1)合成氨反应是一个可逆反应:N2(g)+3H2(g)![]() 2NH3(g),已知298K时:ΔH=-92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据正反应的焓变和熵变分析,常温下合成氨反应____(填“能”或“不能”)自发进行。实验研究表明,在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式如下,v=kc(N2)c1.5(H2)c-1(NH3),k为速率常数,请根据该关系式分析,如果想增大合成氨反应的速率,从浓度的角度可以采用的措施为________。根据合成氨反应的特点,请再说出一项能够提高合成氨反应速率的措施_________。
2NH3(g),已知298K时:ΔH=-92.2kJ/mol,ΔS=-198.2J/(K·mol),则根据正反应的焓变和熵变分析,常温下合成氨反应____(填“能”或“不能”)自发进行。实验研究表明,在特定条件下,合成氨反应的速率与参加反应的物质的浓度的关系式如下,v=kc(N2)c1.5(H2)c-1(NH3),k为速率常数,请根据该关系式分析,如果想增大合成氨反应的速率,从浓度的角度可以采用的措施为________。根据合成氨反应的特点,请再说出一项能够提高合成氨反应速率的措施_________。
(2)研究表明,在Fe催化剂作用下合成氨的反应历程为(*表示吸附态):
化学吸附:N2(g)→2N*;H2(g)→2H*;
表面反应:N*+H*![]() NH*;NH*+H*
NH*;NH*+H*![]() NH2*;NH2*+H*
NH2*;NH2*+H*![]() NH3*
NH3*
脱 附:NH3*![]() NH3(g)
NH3(g)
其中,N2的吸附分解反应速率慢,解决了合成氨的整体反应速率。
实际生产中,合成氨常用工艺条件:Fe作催化剂,控制温度773K,压强3.0×107Pa,原料中N2和H2物质的量之比为1:2.8。请回答:
①分析说明原料中N2过量的理由____________。
②近年来,中国科学院大连化学物理研究所陈平研究团队经过近二十年的积累,先后在催化剂分解、催化氨合成、化学链合成氨等方面取得重要进展。关于合成氨工艺的下列理解,正确的是______。
A.人们对合成氨研究的重要目的之一是要实现氨的低温高效合成
B.控制温度(773K)远于室温,是为了保证尽可能高的平衡转化率和快的反应速率
C.陈平团队首次报道了具有优异低温活性的LiH-3d过渡金属这一复合催化剂体系,它可以大大提高反应的平衡转化率
D.N2的吸附分解反应活化能高,是合成氨反应条件苛刻的重要原因
E.陈平团队构建了一条基于可再生能源的化学链合成氨工艺流程,可以显著提高能效
(3)若N2和H2生成NH3的反应为:![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g),的标准平衡常数
NH3(g),的标准平衡常数 ,其中
,其中![]() 为标准大气压(1×105Pa),
为标准大气压(1×105Pa),![]() 、
、![]() 和
和![]() 为各组分的平衡分压,如P(NH3)=x(NH3) P,P为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。
为各组分的平衡分压,如P(NH3)=x(NH3) P,P为平衡总压,x(NH3)为平衡系统中NH3的物质的量分数。
①N2和H2起始物质的量之比为1:3,反应在恒定温度和标准压强下进行,NH3的平衡产率为![]() ,则
,则![]() _________(用含
_________(用含![]() 的最简式表示)
的最简式表示)
②根据合成氨反应的特点,标准平衡常数![]() 随温度T升高而逐渐______(填“增大”或“减小”)。
随温度T升高而逐渐______(填“增大”或“减小”)。
(4)希腊两位科学家曾经采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶体薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A为______极(填“阴”或“阳”),该极上的电极反应式是___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某中学化学兴趣小组,将一包白色粉末(NaHCO3和Na2CO3的混合物)进行定量分析。现称取一份质量为27.4 g的样品,将此样品加热灼烧至质量不再变化,取出剩余物质,冷却后称重,质量为21.2g。
(1)写出加热时发生反应的化学方程式:___。
(2)分别求出该样品中NaHCO3和Na2CO3的物质的量。____、____(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门实用性很强的科学。根据题意填空:
(1)古代锻造刀剑时,将炽热的刀剑快速投入水中“淬火”,反应为:3Fe+4H2O(g) ![]() Fe3O4+4H2。该反应中H2O作__________(填“氧化剂”或“还原剂”);
Fe3O4+4H2。该反应中H2O作__________(填“氧化剂”或“还原剂”);
(2)某同学炒菜时发现,汤汁溅到液化气的火焰上时,火焰呈黄色。据此他判断汤汁中含有________(填“钠”或“钾”)元素;
(3)海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是__________(填“生石灰”或“盐酸”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是
A. 溶解烧渣选用足量硫酸,试剂X选用铁粉
B. 固体1中一定含有SiO2;控制pH是为了使Al3+转化为A1(OH)3进入固体2
C. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
D. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com