
工业上生产氮化硅陶瓷反应为3SiCl4+2N2+6H2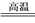 Si3N4+12HCl,有关该反应说法正确的是
Si3N4+12HCl,有关该反应说法正确的是
A. SiCl4是氧化剂 B. N2失电子 C. H2被还原 D. N2发生还原反应
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上学期期末考试(理)化学试卷(解析版) 题型:选择题
工业上常利用CO与SO2反应生成固态S单质和CO2,从而消除这两种气体对大气的污染:2CO(g)+SO2(g) 2CO2(g)+S(s) ΔH=-a kJ/mol(a>0),下列叙述正确的是
2CO2(g)+S(s) ΔH=-a kJ/mol(a>0),下列叙述正确的是
A. 该反应的平衡常数表达式为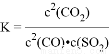
B. 若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ
C. 增大压强或升高温度都可以加快化学反应速率并提高SO2的转化率
D. 若单位时间内生成2 mol CO2,同时消耗1 mol SO2,则说明反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三第二次质检化学试卷(解析版) 题型:简答题
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3•CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中.从废料中回收氧化钴(CoO)的工艺流程如下:
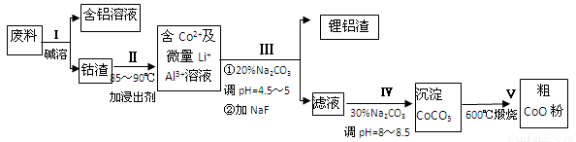
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 .
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的离子反应方程式为 (产物中只有一种酸根).请从反应原理分析不用盐酸浸出钴的主要原因 .
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: .
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:简答题
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖的漂白和杀菌,其一种生产工艺流程如下:
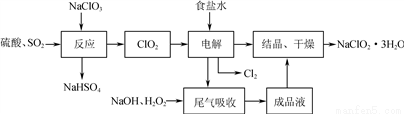
回答下列问题:
(1) 写出“反应”步骤中生成ClO2的化学方程式:________________________。
(2) “电解”所用食盐水由粗盐水精制而成,精制时为除去Mg2+和Ca2+,要加入的试剂分别为___________________、___________________。
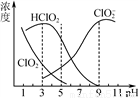
(3) 亚氯酸钠(NaClO2)在水溶液中可生成ClO2、HClO2、ClO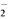 、Cl-等,其中HClO2和ClO2都具有漂白作用。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则使用该漂白剂的适宜pH________(填“大于”“ 等于”或“小于”)3。
、Cl-等,其中HClO2和ClO2都具有漂白作用。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则使用该漂白剂的适宜pH________(填“大于”“ 等于”或“小于”)3。
(4) 为了测定NaClO2·3H2O的纯度,取上述合成产品10.00 g溶于水配成1000 mL溶液,取出20.00 mL溶液于锥形瓶中,再加入足量硫酸酸化的KI溶液,充分反应后加入2~3滴淀粉溶液,用0.2640 mol·L-1Na2S2O3标准溶液滴定,共用去Na2S2O3标准溶液20.00 mL,通过计算确定该产品纯度是否合格?(合格纯度在90%以上)(写出计算过程)__________
提示: 2Na2S2O3+I2===Na2S4O6+2NaI。
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:选择题
下列反应的离子方程式中,书写正确的是
A. 氢氧化铜与稀硫酸反应:OH-+H+===H2O
B. 氯化铝溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH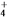
C. 碳酸钙与醋酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
D. 铁粉加入稀硫酸中:2Fe+6H+===2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:选择题
下列有机物属于高分子化合物的是
A. 淀粉 B. 脂肪 C. 乙酸乙酯 D. 蔗糖
查看答案和解析>>
科目:高中化学 来源:2016~2017学年江苏省宿迁市高二学业水平测试模拟(二)化学试卷(解析版) 题型:选择题
在生产生活中,下列不属于化学变化的是
A. 用铁矿石冶炼铁 B. 用铝热反应焊接铁轨
C. 用石油分馏得汽油 D. 氯碱工业制氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省湛江市高二上学期期末调研考试化学试卷(解析版) 题型:简答题
(1)将NaHCO3溶液跟Al2(SO4)3溶液混合,相关反应的离子方程式是____________。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①微粒种类:Na2CO3__________NaHCO3溶液(填“﹥”、“<”或“=”)。
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)____________(填“增大”、“减小”或“不变”);NaHCO3溶液中的c(HCO3-)_________(填“增大”、“减小”或“不变”)。
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲__________________、乙_________________。
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液__________CH3COONa溶液(填“﹥”、“<”或“=”)。
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为__________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省漳州市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列关于反应热的描述中正确的是
A. 由H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ·mol-1可知:含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量为57.3 kJ
B. 由C(石墨,s)===C(金刚石,s) ΔH=1.9 kJ·mol-1,可知:石墨比金刚石更稳定
C. 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
D. 甲烷的标准燃烧热(ΔH)为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com