
| A. | 在硫酸工艺流程中,对尾气中的SO2用过量的氨水吸收的反应2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| B. | FeCl2在空气中被氧化 4Fe2++O2+2H2O=4Fe3++4OH- | |
| C. | AlCl3溶液中通入过量的NH3:Al3++4NH3•H2O=AlO2-+4NH4+ | |
| D. | FeBr2 (aq) 中通入少量Cl2 2Fe2++4Br-+3Cl2=2Fe3++2 Br2+6Cl- |
分析 A.SO2用过量的氨水吸收的反应生成亚硫酸铵;
B.FeCl2在空气中被氧化生成氢氧化铁和氯化铁;
C.氨水为弱碱,二者反应生成氢氧化铝沉淀;
D.FeBr2(aq)中通入少量Cl2,只有亚铁离子被氧化.
解答 解:A.对尾气中的SO2用过量的氨水吸收,反应生成亚硫酸铵,反应的离子反应为:2NH3•H2O+SO2=2NH4++SO32-+H2O,故A正确;
B.FeCl2在空气中被氧化生成氢氧化铁氯化铁,正确的离子方程式为:12Fe2++3O2+6H2O=4Fe(OH)3↓+8Fe3+,故B错误;
C.氢氧化铝不溶于弱碱氨水,反应生成的是氢氧化铝沉淀,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.FeBr2(aq)中通入少量Cl2,氯气先氧化亚铁离子,再氧化溴离子,氯气少量,只有亚铁离子被氧化,正确的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,题目难度中等,明确发生的化学反应及离子反应的书写方法即可解答,B为学生解答中的易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
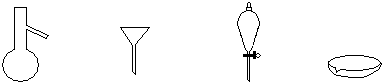
| A. | 蒸馏、蒸发、分液、过滤 | B. | 蒸馏、过滤、分液、蒸发 | ||
| C. | 萃取、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、萃取、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、HCO3-、Cl-、K+ | B. | Al3+、NH4+、CO32-、Cl- | ||
| C. | Ca2+、Na+、NO3-、SO42- | D. | H+、NH4+、I-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为氢氧化钠 | |
| B. | 向FeI2溶液中通入少量Cl2,再滴加少量CCl4,振汤、静置,下层液体为紫色 | |
| C. | 将SO2气体通入溴水,欲检验是否有SO42-生成,可向溶液中滴加Ba(NO3)2溶液 | |
| D. | 一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)△H>0,△S>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、硫酸、Fe2(SO4)3溶液 | B. | NaCl、KCl、AgNO3溶液 | ||
| C. | NaOH溶液、水玻璃 | D. | MnO2、KClO3、KMnO4固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体系颜色比原来深 | B. | 体系颜色比原来浅 | ||
| C. | 体系颜色不变 | D. | 注射器内压强不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com