
【题目】按要求回答下列问题:
(1)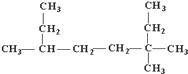 的名称为;
的名称为;
(2)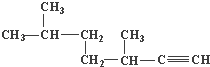 的名称为;
的名称为;
(3)2,4﹣二氯甲苯的结构简式为;
(4)某物质结构如右图 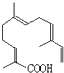 所示,分子式为;该物质可以与下列(填序号)发生反应.
所示,分子式为;该物质可以与下列(填序号)发生反应.
A.KMnO4酸性溶液 B.氢气 C.溴水 D.NaOH溶液
(5)![]() 中含有的官能团的名称为 , .
中含有的官能团的名称为 , .
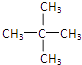
(6)在戊烷的各种同分异构体中,核磁共振氢谱只有一个吸收峰的结构简式为 .
【答案】
(1)3,3,6﹣三甲基辛烷
(2)3,6﹣二甲基﹣1﹣庚炔
(3)
(4)C15H22O2;ABCD
(5)羟基;酯基
(6)
【解析】解:(1) 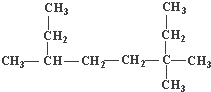 ,该有机物分子中最长碳链含有8个C,主链为辛烷,从右上方开始编号,在3号C含有2个甲基、在6号C含有1个甲基,该有机物名称为:3,3,6﹣三甲基辛烷,
,该有机物分子中最长碳链含有8个C,主链为辛烷,从右上方开始编号,在3号C含有2个甲基、在6号C含有1个甲基,该有机物名称为:3,3,6﹣三甲基辛烷,
所以答案是:3,3,6﹣三甲基辛烷; (2) 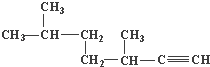 ,该有机物为炔烃,选取含有碳碳三键的最长碳链为主链,该有机物最长碳链含有7个C,主链为庚炔,编号从右边开始,碳碳三键在1号C,在3、6号C各含有1个甲基,该有机物名称为:3,6﹣二甲基﹣1﹣庚炔,
,该有机物为炔烃,选取含有碳碳三键的最长碳链为主链,该有机物最长碳链含有7个C,主链为庚炔,编号从右边开始,碳碳三键在1号C,在3、6号C各含有1个甲基,该有机物名称为:3,6﹣二甲基﹣1﹣庚炔,
所以答案是:3,6﹣二甲基﹣1﹣庚炔;(3)2,4﹣二氯甲苯的主链为甲苯,甲苯所在的C为1号C,在2、4号C各含有一个氯原子,该有机物结构简式为: 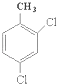 ,
,
所以答案是:  ;(4)该有机物分子中含有15个C、22个H和2个O,该有机物的分子式为:C15H22O2;
;(4)该有机物分子中含有15个C、22个H和2个O,该有机物的分子式为:C15H22O2;
该有机物含有碳碳双键,能够与被酸性高锰酸钾溶液氧化,能够与氢气发生加成反应,能够使溴水褪色;分子中还含有羧基,能够与氢氧化钠溶液发生中和反应,所以ABCD都正确,
所以答案是:C15H22O2;ABCD.(5) ![]() 中含有的官能团为羟基、酯基,
中含有的官能团为羟基、酯基,
所以答案是:羟基;酯基; (6)戊烷的同分异构体有:正戊烷: ![]() 、异戊烷
、异戊烷 ![]() 和新戊烷、
和新戊烷、 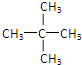 ,其中分子中只有一种等效H一种的为新戊烷:
,其中分子中只有一种等效H一种的为新戊烷:  ,
,
所以答案是:  .
.
【考点精析】根据题目的已知条件,利用有机物的结构和性质和烃的衍生物官能团的相关知识可以得到问题的答案,需要掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解;从结构上说,可以看成是烃分子里的氢原子被其他原子或原子团取代而衍变成的,因此叫烃的衍生物.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写正确的是( )
A.实验室用大理石和稀盐酸制取CO2:2H++CO ![]() =CO2↑+H2O
=CO2↑+H2O
B.铁和稀硝酸反应:Fe+2H+=H2↑+Fe2+
C.向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH﹣=Al(OH)3↓
D.NaHCO3溶液与NaOH溶液反应:OH﹣+HCO ![]() =CO
=CO ![]() +H2O
+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四块金属片,用导线两两相连插入稀硫酸中,可以组成各种原电池。若A和B相连时,A为负极;C与D相连时,C溶解,D上有氢气生成;A与C相连时,C为正极;B与D相连时,电子由D极经导线流向B极,则这四种金属的活泼性由强到弱的顺序为( )
A. ABCDB. ACDBC. CADBD. BDCA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中能大量共存的是( )
A.无色溶液中:K+、Na+、MnO ![]() 、SO
、SO ![]()
B.在酸性溶液中:Ba2+、Na+、SO ![]() 、Cl﹣
、Cl﹣
C.加入Al能放出H2的溶液中:Cl﹣、HCO ![]() 、SO
、SO ![]() 、NH
、NH ![]()
D.含大量Fe2+溶液中:K+、Cl﹣、NO ![]() 、Na+
、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于正在研究和开发的新能源有( )
①生物质能 ②柴草 ③煤炭 ④太阳能 ⑤氢能 ⑥液化石油气 ⑦水煤气 ⑧天然气.
A.①④⑤
B.②③⑥⑦
C.③⑥⑦⑧
D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2 , ②KClO3+6HCl=3Cl2+KCl+3H2O,③2KBrO3+Cl2=Br2+2KClO3 , 下列说法正确的是( )
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 |
H2SO4 | 10.4 | 338 | 吸水性且不易分解 |
实验室用干燥、纯净的二氧化硫和氯气合成硫酰氯,装置如图所示(夹持仪器已省略),请回答有关问题:
(1)仪器A冷却水的进水口为(填“a”或“b”)。
(2)仪器B中盛放的药品是。
(3)实验时,装置丁中发生反应的离子方程式为。
(4)装置丙的作用为 , 若缺少装置乙,则硫酰氯会水解,该反应的化学
方程式为。
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:2ClSO3H=H2SO4+ SO2Cl2 , 此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的方法是。
②请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定方面越来越引起人们的重视,其中氢叠氮酸(HN3)是一种弱酸,分子结构示意图可表示为:
联氨被亚硝酸氧化时便可生成氢叠氮酸(HN3):N2H4+HNO2=2H2O+HN3
它的酸性类似于醋酸,微弱电离出H+和N。试回答下列问题:
(1)下列有关说法正确的是_____________(选填序号)。
A.HN3中含有5个σ键
B.HN3中三个氮原子采用的都是sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.肼(N2H4)沸点高达113.5℃,说明肼分子间可形成氢键
(2)叠氮化物能与Fe3+及Cu2+及Co3+等形成配合物,如:Co[(N3)(NH3)5]SO4 , 在该配合物中钴显价,根据价层互斥理论可知SO空间形状为 , 写出钴原子在基态时的核外电子排布式。
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是_____(选填序号)
A.NaN3与KN3结构类似,前者晶格能较小
B.钠晶胞结构如上图,晶胞中分摊2个钠原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
(4)与N互为等电子体的分子有(举2例)
(5)人造立方氮化硼的硬度仅次于金刚石而远远高于其它材料,因此它与金刚石统称为超硬材料。立方氮化硼晶胞如下图所示,试分析: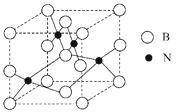
①该晶体的类别为晶体。
②晶体中每个N同时吸引个B。
③设该晶体的摩尔质量为M g·mol-1 , 晶体的密度
为ρg·cm-3 , 阿伏加德罗常数的值为NA , 则晶体
中两个距离最近的B之间的距离为cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com