
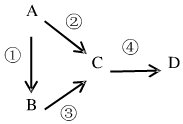
 A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.
A、B、C、D均为中学化学常见物质,且均含有同一种元素,它们之间有如图转化关系,其中A是单质.分析 (1)若A是一种淡黄色固体,B是气态氢化物,C、D为气态氧化物,且C是形成酸雨的主要物质,C为SO2,则A为S,B为H2S,D为SO3,C与B反应生成S和水;
(2)B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因,则C为NO,A为N2,B为NH3,D为NO2;
(3)B、D既能溶于强酸溶液,又能溶于强碱溶液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现,则A为Al,B为Al2O3,C为AlO2-,D为Al(OH)3;
(4)C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱,则C为Na2O2,D为NaOH.
解答 解:(1)若A是一种淡黄色固体,B是气态氢化物,C、D为气态氧化物,且C是形成酸雨的主要物质,C为SO2,则A为S,B为H2S,D为SO3,C与B反应生成S和水,其化学反应为SO2+2H2S=3S↓+2H2O,故答案为:SO2+2H2S=3S↓+2H2O;
(2)B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因,则C为NO,A为N2,B为NH3,D为NO2,反应③的化学方程式4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O;
(3)B、D既能溶于强酸溶液,又能溶于强碱溶液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现,则A为Al,B为Al2O3,C为AlO2-,D为Al(OH)3,则②的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱,则C为Na2O2,D为NaOH,则C作供氧剂时的离子方程式为2Na2O2+2H2O=4OH-+4Na++O2↑,氧化产物为O2,还原产物为2NaOH,所以氧化产物和还原产物的物质的量之比为1:2,
故答案为:1:2.
点评 本题考查无机物的推断,为高频考点,综合考查非金属元素及金属元素化合物性质,涉及常见元素及其化合物知识的考查,把握单质及化合物的性质来分析推断各物质为解答的关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Cu2+为重金属离子,故CuSO4不能用于生活用水消毒 | |
| B. | 卤水煮豆腐是Mg2+、Ca2+等使蛋白质胶体发生凝聚过程 | |
| C. | 纯碱溶液可以洗涤餐具上的油渍 | |
| D. | 油漆刷在钢铁护栏表层用来防止金属锈蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 硫原子的结构示意图: | |
| C. | 基态18O的电子排布式:1s22s22p63s23p6 | |
| D. | CH4分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,NaOH是还原剂 | |
| B. | 每生成1 mol NaClO3转移6 mol电子 | |
| C. | 还原产物是NaClO3,氧化产物是NaCl | |
| D. | 被氧化的氯原子与被还原的氯原子个数比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com